Mini-Organe aus Stammzellen züchten
Im letzten Jahr haben MDC-Forschende funktionsfähiges Muskelgewebe sowie Rückenmarksneuronen, die die Muskelbewegung kontrollieren, aus Stammzellen gezüchtet. Während der „Langen Nacht der Wissenschaften“ können Sie diese Zellen und Gewebe von nahem betrachten und erfahren, warum sie so bedeutend sind.
Zwar ist es inzwischen relativ verbreitet, Gewebe aus Stammzellen zu züchten. Bisher aber war es niemandem gelungen, die Schlüsselelemente des neuromuskulären Systems als Organoide zu züchten – organähnliche Strukturen im Miniformat. Erst in den letzten zwei Jahren ist dies am Max-Delbrück-Centrum für Molekulare Medizin geschehen.
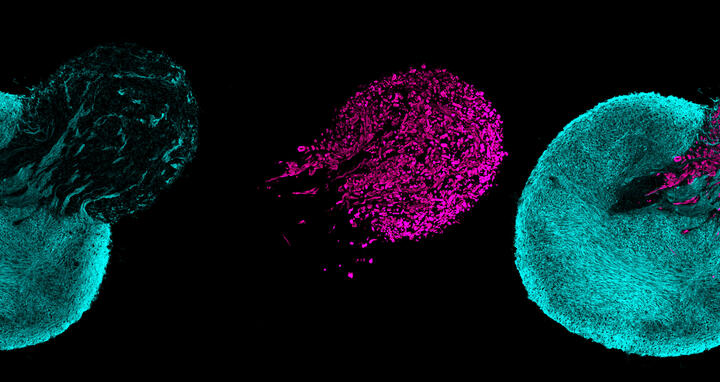
Aus menschlichen Stammzellen können sich dreidimensionale, neuromuskuläre Mini-Organe bilden. Die Rückenmarksneuronen sind hier in einem Blauton zu sehen, die Skelettmuskelzellen sind lila markiert.
„Das ist wirklich Forschung, der wir uns aktuell im Labor widmen”, sagt Dr. Mina Gouti, die die Arbeitsgruppe „Stammzell-Modellierung der Entwicklung und Erkrankung“ am MDC leitet. „Deshalb sind wir ganz begeistert, sie der Öffentlichkeit vorzustellen.”
Erkrankungen erforschen und behandeln
Die neuromuskulären Organoide haben großes Potenzial, wenn es darum geht, die Entwicklung des neuromuskulären Systems und seiner Erkrankungen zu erforschen. Dazu gehören etwa spinale Muskelatrophie und amyotrophe Lateralsklerose (ALS), die auch als „Lou-Gehrig-Krankheit“ bekannt ist.
Bewegungen, die uns selbstverständlich erscheinen – gehen, Kaffee trinken, atmen – setzen Muskelkontraktionen voraus. Sie werden durch eine Botschaft ausgelöst, die die Rückenmarksneuronen senden. Wenn dieses Kommunikationssystem zusammenbricht, führt das zu gravierenden Erkrankungen.
Gouti will die Organoide künftig nutzen, um neue Behandlungsmethoden zu suchen, die beispielsweise den Abbau von Muskelneuronen verlangsamen, verhindern oder vielleicht sogar die Kommunikation zwischen Rückenmark und Muskeln wiederherstellen können. „Das wird ein langwieriger, schwieriger Prozess“, prognostiziert Gouti. „Es ist jedoch sehr vielversprechend.“
Es beginnt mit Stammzellen
Goutis Gruppe züchtet die Organoide aus einem speziellen Stammzellentyp, den induzierten pluripotenten Stammzellen (iPSCs). Molekularbiologen können einem Patienten oder einer Patientin eine Gewebeprobe entnehmen und beispielsweise Hautzellen so umprogrammieren, dass sie wieder zu Stammzellen werden. Dies sind die induzierten pluripotenten Stammzellen. Pluripotente Stammzellen haben die Fähigkeit, sich im Körper zu jeder Art Zelle zu entwickeln. Die Schwierigkeit: Die Wissenschaftlerinnen und Wissenschaftler müssen die iPSCs dazu bringen, sich genau zu jenem Gewebe zu entwickeln, das sie erforschen wollen.
Erst vor etwa einem Jahr brachten Gouti und ihre Mitstreitenden Stammzellen erfolgreich dazu, letztendlich Rückenmarksneuronen und Skelettmuskeln zu bilden und in einer Petrischale zu einer dreidimensionalen, sich selbstorganisierenden Gewebestruktur heranzuwachsen. Der Schlüssel zum Erfolg liegt darin, die Signale und weiteren Einflüsse zu verstehen, die dafür sorgen, dass eine Zelle beispielsweise eine Muskelzelle und keine Hirn- oder Herzzelle werden.
Auf das Individuum zugeschnitten
Wichtig ist: Wozu auch immer sich diese Zellen entwickeln, sie tragen die Mutationen der Patienten-DNA weiterhin in sich und erlauben den Forschenden, die Erkrankung deutlich unkomplizierter im Labor zu untersuchen als am Menschen. Dazu gehören beispielsweise Tests, wie Organoide aus den Zellen des Erkrankten auf bestimmte Arzneimittel oder Behandlungen reagieren.
Zunächst jedoch müssen die Forschenden grundsätzlichere Herausforderungen angehen und beispielsweise die Gewebezellen im Labor über einen längeren Zeitraum hinweg erhalten. Die Organoide können zwar mehrere Monate lang wachsen und beginnen dann zu kontrahieren, ganz wie Muskeln im Körper. Ihnen fehlt jedoch ein komplettes Blutgefäßsystem, das Nährstoffe ins Innere des Miniorgans transportiert. Ihr Wachstum hat also Grenzen. Die Wissenschaftlerinnen und Wissenschaftler müssen außerdem erst verstehen, inwieweit sich das Gewebe von Organoiden mit „echtem“ Gewebe vergleichen lässt.
Wer an der Laborführung teilnimmt, kann Stammzellen unter dem Mikroskop betrachten, fluoreszierende Bilder von Neuronen und Skelettmuskeln sowie die Organoide selbst. Es wird gezeigt, wie das Forschungsteam Gewebe züchtet, pflegt und wie sich die Organoide im Laufe der Zeit zu einem funktions- und kontraktionsfähigen Muskel entwickeln.
Text: Laura Petersen