Angeborene Immunschwäche entdeckt – und aufgeklärt
Gemeinsame Pressemitteilung mit der Charité — Universitätsmedizin Berlin
Bei sieben Kindern mit ausgeprägter Immunschwäche hat ein internationales Konsortium von Forschenden eine übereinstimmende T95R-Mutation im Gen für den Interferon-Regulations-Faktor 4 (IRF4) entdeckt. IRF4 ist ein Transkriptionsfaktor, das Protein steuert also, wieviel Boten-RNA eine Zelle herstellt. Er ist aber auch wichtig während der Entwicklung und Aktivierung von Immunzellen. Die Patient*innen stammen aus sechs nicht verwandten Familien, die auf vier unterschiedlichen Kontinenten leben. Das Team, zu dem die Gruppe von Professor Stephan Mathas und Dr. Martin Janz vom Experimental and Clinical Research Center (ECRC), einer gemeinsamen Einrichtung des Max Delbrück Centers und der Charité – Universitätsmedizin Berlin, gehört, konnte außerdem aufklären, wie sich die Mutation auf das Immunsystem auswirkt. Ein bisher unbeschriebener Mechanismus führt zu einem angeborenen, kombinierten Immundefekt. Darüber berichtet das Konsortium im Fachmagazin „Science Immunology“.
Zum Konsortium gehören neben zwei deutschen Arbeitsgruppen – von der Charité / dem Max Delbrück Center und der Universität Ulm – Forschende der Kinderkliniken und Universitäten in Canberra (Australien), Shanghai (China), Vancouver (Kanada), Paris (Frankreich), Nashville (USA) und den National Institutes of Health in Bethesda (USA).
Immer wieder Infekte der oberen Atemwege
Immundefiziente Kinder leiden immer wieder an Infekten der oberen Atemwege.
Angeborene Immundefekte sind selten und oft unterschiedlich stark ausgeprägt. „Immundefiziente Kinder leiden immer wieder an Infekten der oberen Atemwege“, erklärt Stephan Mathas, Spezialist für die Molekularbiologie von Transkriptionsfaktoren und Leiter der Arbeitsgruppe „Biologie maligner Lymphome“ am ECRC. Es sind häufig Infektionen mit dem Epstein-Barr- oder Zytomegalie-Virus oder mit Pneumocystis jirovecii, einem Erreger, der Lungenentzündungen auslöst; allesamt Infektionen, die Mediziner*innen gut von anderen immungeschwächten Patient*innen kennen.
Auch die sieben Patient*innen leiden unter diesen Infektionen. Bei genauer Untersuchung hat darüber hinaus ihr Immunsystem Gemeinsamkeiten: „Es fiel auf, dass alle Kinder zu wenig Antikörper im Blut haben und sehr wenig B‑Zellen, die normalerweise diese Antikörper produzieren. Zudem ist die Zahl ihrer T‑Zellen und deren Funktionen im Vergleich zu Gesunden reduziert“, sagt Mathas. T‑Zellen sind neben den B‑Zellen und Antikörpern ein wichtiger Arm des Immunsystems.
Bei vielen Kindern mit angeborener Immunschwäche ist die Ursache des Defekts unbekannt, kann aber heutzutage durch Sequenzierung des Genoms ermittelt werden. Auf diese Weise kam auch die IRF4-Mutation T95R zutage. Durch engen Austausch unter Kollegen in internationalen Netzwerken wurde klar, dass es sich bei der genetischen Ursache der Erkrankung dieser Kinder, deren Familien nicht verwandt sind, um die gleiche Punktmutation handelt. Sie sind die Indexpatient*innen, bei denen der Defekt nun erstmals beschrieben wird. Dem internationalen Konsortium ist es zudem gelungen, das gleiche Krankheitsbild auch durch gezielte Mutation des Irf4-Gens bei der Maus zu erzeugen, wodurch es gelang, die durch die IRF4 ausgelösten Fehlfunktionen im Immunsystem im Detail besser zu verstehen.
Spontane Mutation in der Keimbahn
Die Mutation T95R liegt immer nur auf einer der beiden Kopien des Erbguts. Und obwohl die Patient*innen auch immer die gesunde Form von IRF4 bilden, entwickeln sie alle diese Immunschwäche. „Die Biologie der Mutation schlägt quasi die der gesunden Form“, sagt Stephan Mathas. Wie Genomanalysen der Familien ergaben, erbten die Indexpatient*innen die Genveränderung nicht von ihren Eltern, sondern sie trat spontan (de novo) in der Keimbahn oder der frühen embryonalen Entwicklung auf.
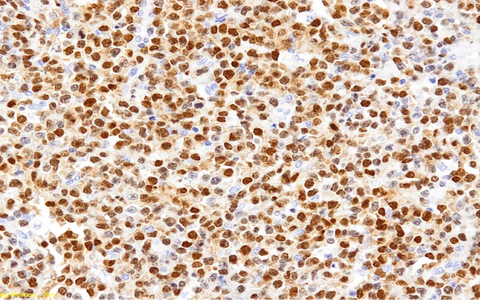
Analyse von IRF4 (in braun gefärbt) in einer Form von Lymphdrüsenkrebserkrankung.
Die Mutation liegt genau an der Stelle des Transkriptionsfaktors IRF4, mit der dieses Protein an die DNA bindet. Statt der ursprünglichen Aminosäure Threonin (T) sitzt dort nun Arginin. „Durch die Mutation verändert sich im Zusammenspiel mit weiteren Faktoren die Affinität von IRF4 für die DNA“, erklärt Stephan Mathas. Das mutierte IRF4-Protein bindet deshalb nicht nur an bekannte DNA-Bindungsstellen je nach Kontext stärker oder schwächer, sondern zudem auch an Stellen des Genoms, wo es gar nicht binden sollte; also Stellen, an denen die normale Variante des Proteins – der Wildtyp – nie haften würde. Durch bioinformatische Analysen gelang es den Forschenden, diese neuen Bindungsstellen zu identifizieren. Die Forschenden beschreiben die Mutation in ihrer Publikation deshalb als „multimorph“, weil nicht nur bestimmte Gene blockiert, sondern andere und sogar neue aktiviert werden.
In den Katalog für die Gendiagnostik aufgenommen
Je nach Art und Ausprägung einer angeborenen Immunschwäche erhalten Betroffene beispielsweise Stammzelltransplantationen oder lebenslange, regelmäßige Injektionen mit Antikörpern. „Die nun publizierte Arbeit lässt vermuten, dass man die Bindungsstellen von mutierten Transkriptionsfaktoren verändern könnte, ohne dabei die gesunde Variante zu beeinflussen“, sagt Stephan Mathas.
Die IRF4-Mutation T95R wird nun jedenfalls in den Katalog der Gene kommen, die zur Diagnostik der angeborenen Immunschwäche gehören. Interessanterweise spielt IRF4 auch bei der Entstehung von bestimmten Blutkrebsarten, an denen Mathas Arbeitsgruppe forscht, eine wichtige Rolle.
Text: Catarina Pietschmann
Weiterführende Informationen
Literatur
IRF4 International Consortium (2023): „A multimorphic mutation in IRF4 causes human autosomal dominant combined immunodeficiency“. Science Immunology, DOI:10.1126/sciimmunol.ade7953
Downloads
Analyse von IRF4 (in braun gefärbt) in einer Form von Lymphdrüsenkrebs.
Credit: Prof. I. Anagnostopoulos, Pathologie Uniklinik Würzburg
Kontakte
Prof. Stephan Mathas
Experimental and Clinical Research Center (ECRC) von Max Delbrück Center und Charité
+49 30 450 553112 (Direktionsassistenz Klinik für Hämatologie, Onkologie und Tumorimmunologie, Campus Charité Mitte)
stephan.mathas@charite.de
Christina Anders
Redakteurin, Abteilung Kommunikation
Max Delbrück Center
+49 30 9406 – 2118
christina.anders@mdc-berlin.de oder presse@mdc-berlin.de
- Max Delbrück Center
-
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (Max Delbrück Center) gehört zu den international führenden biomedizinischen Forschungszentren. Nobelpreisträger Max Delbrück, geboren in Berlin, war ein Begründer der Molekularbiologie. An den Standorten in Berlin-Buch und Mitte analysieren Forscher*innen aus rund 70 Ländern das System Mensch – die Grundlagen des Lebens von seinen kleinsten Bausteinen bis zu organ-übergreifenden Mechanismen. Wenn man versteht, was das dynamische Gleichgewicht in der Zelle, einem Organ oder im ganzen Körper steuert oder stört, kann man Krankheiten vorbeugen, sie früh diagnostizieren und mit passgenauen Therapien stoppen. Die Erkenntnisse der Grundlagenforschung sollen rasch Patient*innen zugutekommen. Das Max Delbrück Center fördert daher Ausgründungen und kooperiert in Netzwerken. Besonders eng sind die Partnerschaften mit der Charité – Universitätsmedizin Berlin im gemeinsamen Experimental and Clinical Research Center (ECRC) und dem Berlin Institute of Health (BIH) in der Charité sowie dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK). Am Max Delbrück Center arbeiten 1800 Menschen. Finanziert wird das 1992 gegründete Max Delbrück Center zu 90 Prozent vom Bund und zu 10 Prozent vom Land Berlin.