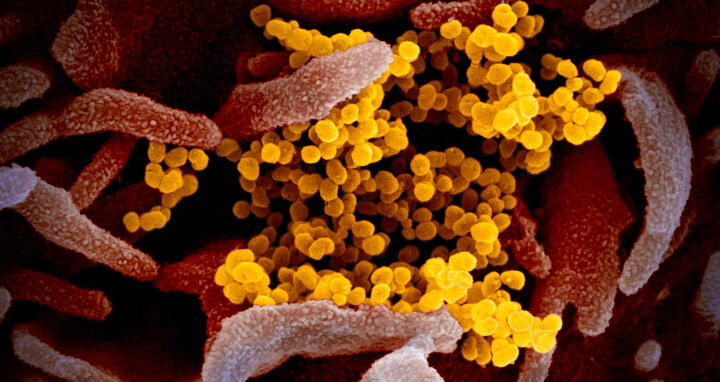
Die Eintrittspforten für SARS-CoV‑2
Dass Forscher*innen des Wellcome Sanger Institutes, des Universitätsklinikums Groningen, der Universität Cote d’Azur und des CNRS in Nizza und ihre Kolleg*innen des Human Cell Atlas Lung Biological Network diese Zellen identifiziert haben, könnte zur Erklärung der hohen Übertragungsrate von SARS-CoV‑2 beitragen.
Die erste Veröffentlichung mit dem Lung Biological Network ist ein Teil der laufenden internationalen Bemühungen, die Daten des Human Cell Atlas zum Verständnis von Infektion und Krankheit zu nutzen, berichten sie heute (am 23. April) im Fachjournal „Nature Medicine“. Darüber hinaus zeigt die Publikation, dass Zellen im Auge und in einigen anderen Organen wie dem Herzen ebenfalls diese Eintrittspforten für die Viren aufweisen. Sie sagt voraus, wie ein wichtiges Eintrittsprotein zusammen mit anderen Genen des Immunsystems reguliert wird und offenbart mögliche Ziele, über die ein Medikament die Übertragung des Virus erschweren könnte.
COVID-19 – die Abkürzung steht für die Coronavirus-Erkrankung (engl.: corona virus disease), die SARS-CoV‑2 auslöst – beeinträchtigt vor allem die Lunge und die Atemwege. Die Symptome der Patient*innen können grippeähnlich sein, mit Fieber, Husten und Halsschmerzen, während andere Menschen gar keine Symptome bemerken, aber dennoch Viren übertragen können. In den schlimmsten Fällen verursacht das Virus eine Lungenentzündung, die bis zum Tod führen kann. Man geht davon aus, dass sich das Virus über Tröpfchen verbreitet, die beim Husten oder Niesen einer infizierten Person entstehen, und es ist anscheinend leicht übertragbar. Bislang hat sich das Virus mehr als 176.000 Menschenleben gefordert.
Welche Zelltypen sind an der Infektion beteiligt?
Wissenschaftler*innen in aller Welt wollen genau verstehen, wie das Virus funktioniert, um die Übertragung zu verhindern und einen Impfstoff zu entwickeln. Dass SARS-CoV‑2 unsere Zellen über einen ähnlichen Mechanismus infiziert wie ein verwandtes Coronavirus, das die SARS-Epidemie im Jahr 2003 verursachte, ist bekannt. Doch die genauen Zelltypen, die in der Nase beteiligt sind, waren zuvor noch nicht genau bestimmt worden.
Die Forscher*innen analysierten daher verschiedene Datensätze des Human Cell Atlas (HCA)-Konsortiums, die aus der Einzelzell-RNA-Sequenzierung von mehr als 20 verschiedenen Geweben nicht infizierter Menschen gewonnen worden waren. Dazu gehörten Zellen aus der Lunge, Nasenhöhle, Auge, Darm, Herz, Niere und Leber. Die Forscher untersuchten, welche der einzelnen Zellen die beiden wichtigsten Eintrittsproteine exprimieren, die das Virus für die Infektion nutzt.
Dr. Waradon Sungnak, der Erstautor der Studie vom Wellcome Sanger Institute, sagt: „Das Rezeptorprotein – ACE2 – und die TMPRSS2-Protease, die beim Eintritt von SARS-CoV‑2 helfen kann, wird in den Zellen verschiedener Organe exprimiert. Darunter sind die Zellen an der Innenseite der Nase. Wir haben dann gezeigt, dass von allen Zellen die schleimproduzierenden Becherzellen und Flimmerzellen in der Nase die höchsten Konzentrationen dieser beiden Proteine aufweisen. Das macht diese Zellen zum wahrscheinlichsten Erstinfektionsweg für das Virus.“
Die Zellen der Nase sind für das Virus leicht zu erreichen
Dr. Martijn Nawijn vom Universitätsklinikum Groningen in den Niederlanden erklärte für das HCA Lung Biological Network: „Diese speziellen Zellen in der Nase sind jetzt erstmals mit COVID-19 in Verbindung gebracht worden. Natürlich gibt es viele Faktoren, die die Übertragbarkeit des Virus beeinflussen. Aber unsere Ergebnisse passen gut mit den bisher beobachteten rasanten Infektionsraten des Virus zusammen. Die Lage dieser Zellen an der Oberfläche der Naseninnenseite macht sie für das Virus leicht zugänglich und kann bei der Übertragung auf andere Menschen helfen.“
Die beiden wichtigsten Eintrittsproteine ACE2 und TMPRSS2 sind auch in Hornhaut-Zellen des Auges und in der Darmschleimhaut zu finden. Dies deutet auf einen weiteren möglichen Infektionsweg über das Auge bzw. die Tränendrüsen hin und offenbart das Potenzial für eine fäkal-orale Übertragung.
Wenn Zellen geschädigt werden oder eine Infektion bekämpfen, werden außerdem verschiedene Immungene aktiviert. Die Studie zeigte, dass die Produktion des ACE2-Rezeptors in den Nasenzellen wahrscheinlich gleichzeitig mit diesen anderen Immungenen angeschaltet wird.
ACE2 ist auch im Herzen zu finden
Wir können auf einzigartige Datensets aus der Einzelzellsequenzierung zurückgreifen.
Bis zu 20 Prozent der im Krankenhaus behandelten COVID-19-Patient*innen erleiden Schäden des Herzmuskels bis hin zum Herzversagen. Es war daher entscheidend, auch für das Herz die Genexpression des SARS-CoV-2-Rezeptors und der helfenden Protease zu kartieren. „Wir haben mehr als 500.000 Einzelzellen aus 14 menschlichen Herzen analysiert. Dabei haben wir die zellulären Bereiche identifiziert, die diese Eintrittspforte expremieren: Das sind Perizyten – also Zellen, die zum feinen Kapillarsystem des Herzens gehören –, Herzmuskelzellen und Fibroblasten, die dazu beitragen, dem Herzen seine Struktur zu geben“, sagt Dr. Michela Noseda vom National Heart & Lung Institute des Imperial College in London. „Das Wissen, auf welche Zellen im Herzen das Virus genau abzielt, ist die Grundlage, um die Mechanismen der Schädigung zu verstehen und über eine Behandlung zu entscheiden.“
„Wir können auf einzigartige Datensets aus der Einzelzellsequenzierung zurückgreifen“, sagt Professor Norbert Hübner, der Leiter der Arbeitsgruppe „Genetik und Genomik kardiovaskulärer Erkrankungen“ am Max-Delbrück-Centrum für Molekulare Medizin (MDC) und zusätzlich Projekte am Deutschen Zentrum für Herz-Kreislaufforschung (DZHK) und am Berlin Institute of Health (BIH) leitet. Gemeinsam mit Jonathan Seidman, Bugher Professor für Kardiovaskuläre Genetik an der Harvard Medical School, koordiniert er ein Team von 13 Wissenschaftlerinnen und Wissenschaftlern aus Deutschland, Großbritannien und den USA, die das menschliche Herz Zelle für Zelle verstehen wollen. Zu dieser Gruppe gehören auch Michela Noseda und Sarah Teichmann. „Den ACE2-Rezeptor haben wir vor allem bei den Perizyten gefunden. Der Rezeptor spielt vermutlich eine grundlegende Rolle dabei, den Blutfluss im Körper aufrecht zu erhalten. Seine Rolle bei den Herzproblemen von COVID-19-Patient*innen ist dagegen eine andere Sache. Wir wissen noch nicht, ob das Virus selbst die Schäden am Herzen verursacht oder ob es sich um sekundäre Effekte handelt.“
Den Human Cell Atlas nutzen, um COVID-19 zu verstehen
Die Studie ist ein Ergebnis des weltweiten Human Cell Atlas-Konsortiums. Das Konsortium will Referenzkarten für alle menschlichen Zellen erstellen, um Gesundheit und Krankheit zu verstehen. Mehr als 1.600 Forscher*innen in 70 Ländern beteiligen sich am Human Cell Atlas (HCA), die Daten stehen Wissenschaftler*innen weltweit offen zur Verfügung.
Dr. Sarah Teichmann, eine Senior-Autorin der Studie vom Wellcome Sanger Institute und Ko-Vorsitzende des HCA-Organisationskomitees, sagt: „Noch während wir den Human Cell Atlas aufbauen, wird er bereits dafür genutzt, COVID-19 zu verstehen und um die Zellen zu identifizieren, die für die erste Infektion und die Übertragbarkeit entscheidend sind. Diese Informationen können genutzt werden, um die Ausbreitung des Coronavirus besser zu verstehen. Das Wissen um die genauen Zelltypen, die für die Virusübertragung wichtig sind, bietet eine Grundlage, um potenzielle Therapien zu entwickeln und die Ausbreitung des Virus zu reduzieren.“
Das globale HCA Lung Biological Network analysiert weiterhin die Daten. Das Netzwerk will weitere Hinweise auf Zellen und Ziele gewinnen, die wahrscheinlich an COVID-19 beteiligt sind, und sie mit den Eigenschaften von Patient*innen abgleichen.
Professor Sir Jeremy Farrar, Direktor von Wellcome, sagt: „Indem er die Merkmale jedes einzelnen Zelltyps bestimmt, hilft der Human Cell Atlas Wissenschaftler*innen, Krankheiten wie COVID-19 auf eine völlig neue Art und Weise zu diagnostizieren, zu überwachen und zu behandeln. Forscher*innen auf der ganzen Welt arbeiten in beispiellosem Tempo daran, unser Verständnis von COVID-19 zu vertiefen. Diese neue Arbeit ist ein Beweis dafür. Die Zusammenarbeit über Grenzen hinweg und der offene Austausch von Forschungsergebnissen ist entscheidend für die rasche Entwicklung wirksamer Diagnostika, Therapien und Impfstoffe und um sicherzustellen, dass kein Land zurückgelassen wird.“
Die Studie wurde von Wellcome, der Chan-Zuckerberg-Initiative, der Europäischen Kommission und anderen Förderern unterstützt. Die komplette Liste ist in der Studie zu finden.
Weiterführende Informationen
- Weitere Forschung des HCA zu COVID-19 unter: https://www.humancellatlas.org/covid-19/
- Die Daten sind zugänglich unter: https://www.covid19cellatlas.org
- MDC-Pressemitteilung: „Mitten ins Herz“
-
MDC / DZHK-Pressemitteilung: „Herzzellen ihre Geheimnisse entlocken“
Literatur
Waradon Sungnak et al. (2020): „Single-Cell Transcriptomics Data Survey Reveals SARS-CoV‑2 Entry Factors Highly Expressed in Nasal Epithelial Cells Together with Innate Immune Genes“. Nature Medicine. DOI: 10.1038/s41591-020‑0868‑6.
Kontakte
Dr. Samantha Wynne
Pressesprecherin
Wellcome Sanger Institute
+44 – 1223 492368
press.office@sanger.ac.uk
Professor Norbert Hübner
Leiter der Arbeitsgruppe „Genetik und Genomik kardiovaskulärer Erkrankungen“
Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC)
nhuebner@mdc-berlin.de
Jana Schlütter
Redakteurin, Abteilung Kommunikation
Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC)
+49 – 30-9406 – 2121
jana.schluetter@mdc-berlin.de
Der Human Cell Atlas
Der Human Cell Atlas (HCA) ist ein internationales gemeinschaftliches Konsortium. Sein Ziel sind umfassende Referenzkarten aller menschlichen Zellen — den grundlegenden Einheiten des Lebens. Diese Karten schaffen die Basis, um die menschliche Gesundheit zu verstehen und für die Diagnose, Überwachung und Behandlung von Krankheiten. Der HCA wird von einem Organisationskomitee geleitet, dessen Ko-Vorsitzende Dr. Sarah Teichmann vom Wellcome Sanger Institute (UK) und Dr. Aviv Regev vom Broad Institute des MIT und Harvard (USA) sind. www.humancellatlas.org
Das Human Cell Atlas Lung Biological Network ist ein Zusammenschluss von 71 Wissenschaftler*innen, die gemeinsam an der Kartierung der Atemwegszellen in unserem Körper arbeiten. Diese Gruppe wird von Dr. Martijn Nawijn, Dr. Pascal Barbry, Dr. Alexander Misharin und Dr. Jayaraj Rajagopal koordiniert.
- Das Max-Delbrück-Centrum für Molekulare Medizin (MDC)
-
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft gehört zu den international führenden biomedizinischen Forschungszentren. Nobelpreisträger Max Delbrück, geboren in Berlin, war ein Begründer der Molekularbiologie. An den MDC-Standorten in Berlin-Buch und Mitte analysieren Forscher*innen aus rund 60 Ländern das System Mensch – die Grundlagen des Lebens von seinen kleinsten Bausteinen bis zu organübergreifenden Mechanismen. Wenn man versteht, was das dynamische Gleichgewicht in der Zelle, einem Organ oder im ganzen Körper steuert oder stört, kann man Krankheiten vorbeugen, sie früh diagnostizieren und mit passgenauen Therapien stoppen. Die Erkenntnisse der Grundlagenforschung sollen rasch Patient*innen zugutekommen. Das MDC fördert daher Ausgründungen und kooperiert in Netzwerken. Besonders eng sind die Partnerschaften mit der Charité – Universitätsmedizin Berlin im gemeinsamen Experimental and Clinical Research Center (ECRC) und dem Berlin Institute of Health (BIH) in der Charité sowie dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK). Am MDC arbeiten 1600 Menschen. Finanziert wird das 1992 gegründete MDC zu 90 Prozent vom Bund und zu 10 Prozent vom Land Berlin.