Wie Zellen auf Medikamente wirklich reagieren
G‑Protein-gekoppelte Rezeptoren (GPCRs), die sich in Zellmembranen befinden und Signale von außen ins Innere der Zellen weiterleiten, werden oft als einfache Schalter beschrieben: Bindet ein Molekül, zum Beispiel ein Neurotransmitter oder ein Hormon, an sie, löst das im Inneren der Zelle eine dominoartige Kettenreaktion aus – eine Signalkaskade, die eine bestimmte Zellfunktion zur Folge hat.
Eine Studie, die Dr. Romy Thomas, ehemalige Doktorandin in der Arbeitsgruppe „Signalprozesse von Rezeptoren“ des Max Delbrück Center und jetzt Postdoktorandin an der Stanford University, gemeinsam mit Kolleg*innen der Universitätsmedizin Mainz und der Universität Leipzig im Fachblatt „Nature“ veröffentlicht hat, deutet nun auf einen komplexeren Mechanismus hin. Die Forschenden zeigen, dass GPCRs in Zellen mehrere Aktivierungswege einschlagen können – wobei verschiedene Moleküle denselben Rezeptor in unterschiedliche aktive Zustände versetzen, die bestimmte Signalwege gegenüber anderen begünstigen.
„Wir haben festgestellt, dass GPCRs sich nicht wie einfache Ein/Aus-Schalter verhalten“, sagt der Letztautor der Studie, Professor Andreas Bock, ehemaliger kommissarischer Leiter der Arbeitsgruppe „Signalprozesse von Rezeptoren“ und jetzt Direktor des Instituts für Pharmakologie am Universitätsklinikum Mainz. „Stattdessen nehmen sie je nach Molekül, das an sie bindet, unterschiedliche Formen an – und jede Konformation löst einen ganz bestimmten Signalweg aus“, erklärt Bock.
Die Arbeitsgruppe „Signalprozesse von Rezeptoren“ hatte einst Professor Martin Lohse gegründet, der ebenfalls zu den Autor*innen der Studie gehört. Von 2016 bis 2019 war Lohse Wissenschaftlicher Vorstand des Max Delbrück Center, heute ist er Geschäftsführer der Forschungsunternehmens ISAR Bioscience in Planegg nahe München.
Rezeptorbewegungen in lebenden Zellen
Frühere Studien hatten bereits gezeigt, dass GPCRs zwischen mehreren inaktiven und aktiven Konformationen wechseln können. Diese Erkenntnisse stammen jedoch aus Experimenten mit isolierten Rezeptoren, die man in künstliche Zellmembranen eingebettet hatte. Die Erforschung solcher Wechsel in lebenden Zellen galt damals als schwierig, da man die subtilen Konformationsänderungen mit den vorhandenen Techniken nicht in ausreichender Präzision erfassen konnte.
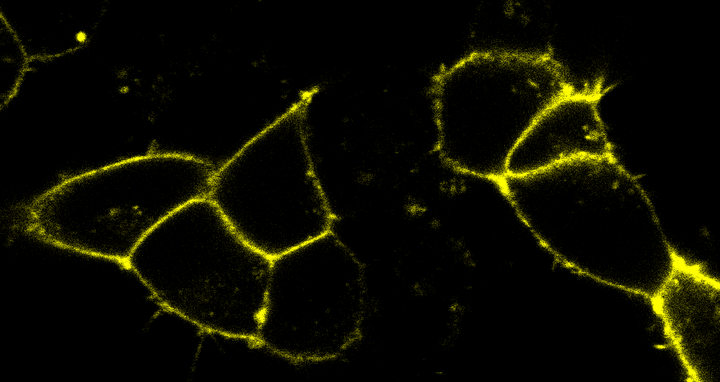
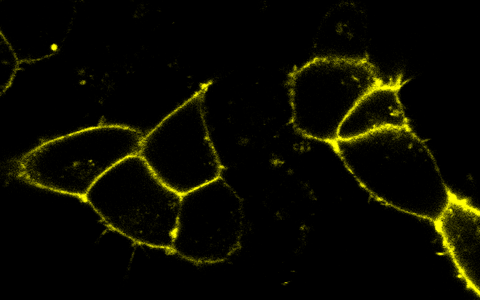
Die Zellmembranen menschlicher Nierenzellen sind mit fluoreszierenden Biomarkern markiert. So ist zu sehen, wie G‑Protein-gekoppelte Rezeptoren ihre Aktivität verändern, wenn Moleküle wie Neurotransmitter oder Hormone an sie binden.
Das Team um Thomas nutzte für die aktuelle Studie den muskarinischen Acetylcholin-Rezeptor M2 als Modell und befestigte – in lebenden Zellen – an präzisen Positionen des Rezeptors winzige fluoreszierende Sonden. Die Technologie hierfür hatte Professorin Irene Coin vom Institut für Biochemie der Universität Leipzig entwickelt. Aktivierten die Forschenden die so markierten Rezeptoren mit unterschiedlichen Substanzen, rief jede einzelne von ihnen spezifische Veränderungen in der Fluoreszenz hervor. Jede Substanz löste demnach sehr individuelle, winzige Bewegungen des Rezeptormoleküls aus und versetzte es so in einen einzigartigen aktiven Zustand. Jeder dieser Zustände wiederum stieß in der Zelle eine Reihe spezifischer biochemischer Reaktionen an.
Bock betont, er verdanke es Lohse, dass dieser ihn und Irene Coin zusammengebracht habe: „Es war Martin Lohse, der mir vorgeschlagen hat, Irene zu treffen und mit ihr an etwas Größerem zusammenzuarbeiten“, erzählt der Forscher. „Er stand uns als einer unserer wichtigsten Ansprechpartner für unsere jahrelange Forschung zur Verfügung und hat uns geholfen, das Konzept dafür zu entwickeln.“
Bessere Medikamente entwickeln
GPCRs steuern zahlreiche Prozesse wie die Herzfrequenz, die Signalübertragung im Gehirn und Reaktionen auf Hormone. Mehr als ein Drittel aller zugelassenen Arzneimittel wirken auf sie ein. „Unsere Studie könnte helfen zu erklären, warum Medikamente, die auf denselben Rezeptor abzielen, sehr unterschiedliche Wirkungen haben können“, sagt Romy Thomas. „Sie schalten den Rezeptor nicht einfach nur ein – sie lenken ihn auf einzigartige Wege.“
„Wir gehen davon aus, dass ähnliche Aktivierungsprozesse auch in vielen anderen Rezeptoren ablaufen“, fügt Coin hinzu. „Unsere Biosensoren könnten dabei helfen, Verbindungen zu identifizieren, die sich auf ganz bestimmte Signalwege der Zelle auswirken oder spezielle Proteine bevorzugt aktivieren.“
Auf der Suche nach neuen Medikamenten könnten Forschende daher künftig nicht nur untersuchen, ob ein Wirkstoff einen Rezeptor aktiviert, sondern auch, wie er diesen verändert und welche Signale das in den Zellen auslöst. Diese Informationen würden helfen, Arzneimittel zu entwickeln, die präziser wirken und weniger unerwünschte Effekte haben.
Text: Gunjan Sinha und Universität Leipzig
Die Studie wurde vom Sonderforschungsbereich (SFB) 1423 „Strukturelle Dynamik der GPCR-Aktivierung und ‑Signaltransduktion“ der Universität Leipzig unterstützt und begann 2019 als Kooperationsprojekt mit dem Max Delbrück Center und der Charité – Universitätsmedizin Berlin.
Weitere Informationen
- Pop-up-Fabriken hinter der Zellmembran
- SFB 1423 (auf Englisch)
- Pressemitteilung der Universität Leipzig
- Pressemitteilung der Universitätsmedizin Mainz
Literatur
Romy Thomas, Pauline Jacoby, Chiara De Faveri, et. al. (2026) “Ligand-specific activation trajectories dictate GPCR signaling in cells,” Nature. DOI: 10.1038/s41586-025 – 09963‑3
Bild zum Download
Die Zellmembranen menschlicher Nierenzellen sind mit fluoreszierenden Biomarkern markiert. So ist zu sehen, wie G‑Protein-gekoppelte Rezeptoren ihre Aktivität verändern, wenn Moleküle wie Neurotransmitter oder Hormone an sie binden.
© Universität Mainz, Romy Thomas
Kontakte
Prof. Dr. Andreas Bock
Direktor des Instituts für Pharmakologie
Universitätsmedizin Mainz
andreas.bock@uni-mainz.de
Nadine Berger
Medienarbeit, Wissenschaftskommunikation
Universitätsmedizin Mainz
+49 6131 17 – 8434
Nadine.Berger@unimedizin-mainz.de
Nina Vogt
Social-Media-Referentin, Stabsstelle Universitätskommunikation
Universität Leipzig
+49 341 97 – 35026
presse@uni-leipzig.de
Gunjan Sinha
Radakteurin Kommunikation
Max Delbrück Center
+49 30 9406 – 2118
Gunjan.Sinha@mdc-berlin.de oder presse@mdc-berlin.de
- Max Delbrück Center
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft legt mit seinen Entdeckungen von heute den Grundstein für die Medizin von morgen. An den Standorten in Berlin-Buch, Berlin-Mitte, Heidelberg und Mannheim arbeiten unsere Forschenden interdisziplinär zusammen, um die Komplexität unterschiedlicher Krankheiten auf Systemebene zu entschlüsseln – von Molekülen und Zellen über Organe bis hin zum gesamten Organismus. In wissenschaftlichen, klinischen und industriellen Partnerschaften sowie in globalen Netzwerken arbeiten wir gemeinsam daran, biologische Erkenntnisse in praxisnahe Anwendungen zu überführen – mit dem Ziel, Frühindikatoren für Krankheiten zu identifizieren, personalisierte Behandlungen zu entwickeln und letztlich Krankheiten vorzubeugen. Das Max Delbrück Center wurde 1992 gegründet und vereint heute eine vielfältige Belegschaft mit rund 1.800 Menschen aus mehr als 70 Ländern. Wir werden zu 90 Prozent durch den Bund und zu 10 Prozent durch das Land Berlin finanziert.