Die Rolle des TRAPP Tethering-Komplexes im Vesikeltransport
Die Rolle des TRAPP Tethering-Komplexes im Vesikeltransport
Der vesikuläre Transport in eukaryontischen Zellen ist ein Beispiel für die modulare Organisation von zellulären Aktivitäten. Dabei werden in sequentieller Abfolge Vesikelknospung und Uncoating an einer Donormembran, sowie Tethering (Anheftung) und Membranfusion an der Zielmembran von funktionell konservierten Ensembles von Proteinen vermittelt. Der heteromultimere Tethering-Komplex TRAPP (Transport Protein Partikel) agiert dabei als Nukleotid-Austauschfaktor für GTPasen der Ypt/Rab Familie vor der Fusion von am ER gebildeten Vesikeln mit dem Golgi. Wir verfolgen einen Ansatz, der biochemische und strukturbiologische Methoden kombiniert, um die Rolle von TRAPP im Vesikeltransport zu untersuchen.
In unserer bisherigen Arbeit haben wir die Kristallstrukturen der TRAPP-Untereinheiten Bet3 und Tpc6 aufgeklärt. Trotz sehr geringer Konservierung der Sequenz bildeten beide Proteine strukturell sehr ähnliche Homodimere, was eine mögliche Heterodimerisierung nahelegte. Durch Co-Expression beider Gene in E. coli konnte tatsächlich ein Bet3-Tpc6 Heterodimer produziert und kristallisiert werden. Die Röntgenstrukturanalyse bestätigte die vorhergesagte Struktur dieses Subkomplexes, der ein zentrales Fragment in der Architektur des TRAPP Komplexes darstellen könnte. Des weiteren konnten Hinweise auf Bindungsstellen von weiteren TRAPP Untereinheiten erhalten werden.
In allen bisher bestimmten Kristallstrukturen von Bet3 hat sich gezeigt, dass dieses Protein stets durch die Verknüpfung einer Fettsäure über eine Thioester-Bindung mit seinem konservierten Cystein 68 modifizeirt ist. Dabei ist die Acylkette in einem hydrophoben Tunnel im Inneren des Proteins verborgen. Wir konnten zeigen, dass dies das Ergebnis einer einzigartigen Selbst-Acylierungsaktivität ist, welche es Bet3 ermöglicht, sich auch in Abwesenheit von Acyl-Transferasen selbst zu palmitoylieren. Der Fettsäuretransfer von Palmitoyl-CoA auf den Cysteinrest kann durch Mutationen, die den hydrophoben Kanal blockieren, verhindert werden. Die Palmitoylierung vermittelt nicht die Membranverankerung von Bet3 mit dem Golgi, sondern stabilisiert das Protein, was in vitro und in vivo beobachtet werden kann.
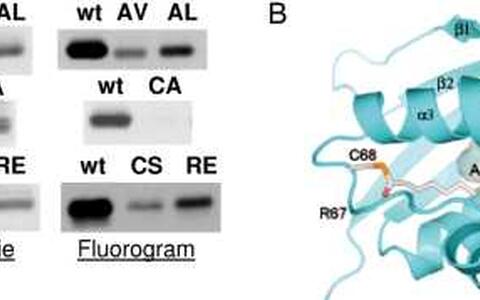
Palmitoylierung der TRAPP Untereinheit Bet3 an Cystein 68. (A) Gleiche Mengen GST-Wildtyp Bet3 und Mutanten mit dem Austausch der Reste A82, C68 bzw. R67 (links) wurden mit [3H]-Palmitoyl-CoA inkubiert. Das Fluorogramm (rechts) zeigt das die Palmitoylierung absolut von der Anwesenheit des Cysteins an Position 68 abhängt und durch die kanalblockierende Mutation an Position 82 oder Ladungsumkehr an Position 67 deutlich reduziert wird. (B) Die Palmitoylkette ist in einem tiefen Kanal im Inneren von Bet3 gebunden, was durch die Einführung von sperrigen Seitenketten an Position 82 verhindert werden kann. Aus Kümmel et al. (2006) Proc. Natl. Acad. Sci. USA 103, 12701 – 12706.