Ein Fehler in den Proteinfabriken des Herzens
Eine krankhafte Zunahme der Herzmuskelmasse gilt als die häufigste Ursache für den plötzlichen Herztod. Wie es zu dieser Herzhypertrophie kommen kann, hat jetzt ein Team um Professor Norbert Hübner, Leiter der Arbeitsgruppe „Genetik und Genomik von Herz-Kreislauferkrankungen“ am Berliner Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC), herausgefunden. Auch die MDC-Arbeitsgruppe „Nicht-kodierende RNAs und Mechanismen der Genregulation im Cytoplasma“ von Dr. Marina Chekulaeva war an der Studie beteiligt.
Die Wissenschaftler*innen haben einen komplexen molekularen Mechanismus entschlüsselt, der die gesamte Proteinproduktion in den Ribosomen der Herzzellen stört. Das Herz bekommt also nicht die Eiweiße, die es eigentlich braucht. Dieser Herstellungsfehler wiederum fördert das abnorme Wachstum der Herzmuskelzellen. Veröffentlicht ist die Studie, an der 19 Forschende aus sechs Ländern mitgearbeitet haben, in der Fachzeitschrift „Genome Biology“.
Die komplette Eiweißproduktion ist beeinträchtigt
„Wir wollten herausfinden, wie natürliche genetische Variationen, die jedes Lebewesen aufweist, zur Entstehung komplexer Krankheiten beitragen können“, sagt Dr. Sebastiaan van Heesch, der gemeinsam mit Hübner Letztautor der Studie in „Genome Biology“ ist. Bis Juni 2020 gehörte der Niederländer als Postdoktorand zu Hübners Arbeitsgruppe am MDC. Inzwischen forscht van Heesch mit einer eigenen Arbeitsgruppe wieder in seinem Heimatland, am Prinses Máxima Centrum für Pädiatrische Onkologie in Utrecht.
„Bekannt war bereits, dass Abweichungen im Erbgut beeinflussen können, ob und wie die Gene im Zellkern abgelesen werden“, sagt van Heesch. Dieser Transkription genannte Prozess ist der erste Schritt auf dem Weg zur Proteinherstellung. Veränderungen der DNA, die zur Herstellung einzelner fehlerhafter Proteine des Herzens führen, kannte man ebenfalls. „Aber dass es tatsächlich genetische Variationen gibt, die sich auf die komplette Proteinproduktion in den Ribosomen, den zellulären Eiweißfabriken, des Herzgewebes auswirken, war neu und auch für uns ziemlich überraschend“, sagt van Heesch.
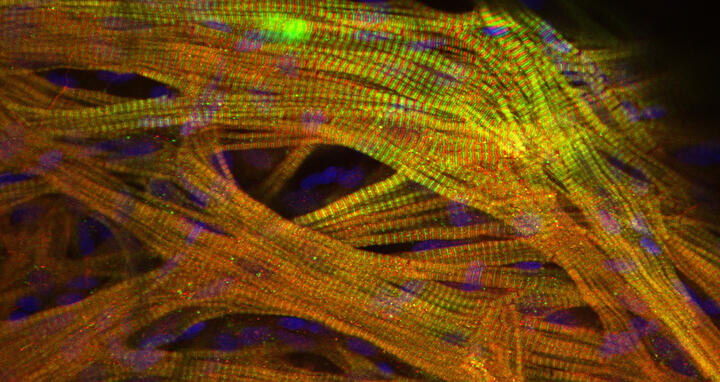
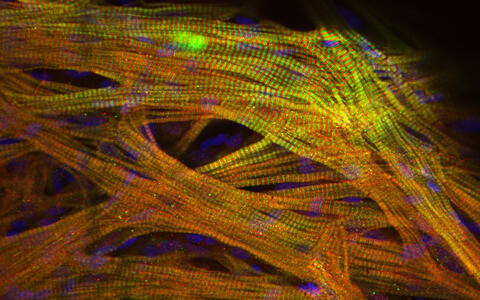
Die Herzmuskelfasern sind als bälkchenartige Gewebestruktur (Trabekeln) angeordnet, damit sich die Herzkammer kraftvoll zusammenzuziehen kann. Wie die verschiedenen Schichten des Herzmuskels im er-wachsenen Organ organisiert sind und wie sie mitei-nander kommunizieren, ist weitgehend unbekannt. Grün sind die Z‑Scheiben der kleinsten funktionellen Einheit des Muskels, den Sarkomeren, und in blauer Farbe die Zellkerne einer transgenen Zebrafisch-Linie dargestellt.
Für lange Proteine besonders verheerend
„Wir haben für unsere Studie mit einer Gruppe von Ratten gearbeitet, von der wir alle genetischen Variationen kennen und zudem wissen, dass etwa die Hälfte der Tiere dieser Kreuzungen ein Herzleiden entwickelt“, berichtet Dr. Jorge Ruiz-Orera aus der gleichen Arbeitsgruppe. Ruiz-Orera ist gemeinsam mit Dr. Franziska Witte, die während der ersten Jahre der Studie Doktorandin im Labor von Hübner war und mittlerweile bei dem Berliner Forschungsunternehmen Nuvisan arbeitet, Erstautor*in der Studie.
Besonders bemerkenswert ist, dass ähnliche Erbgutvariationen auch bei anderen Arten – etwa bei Mäusen, Menschen und sogar bei einzelligen Organismen wie der Hefe – die gleichen Effekte auf die Proteinsynthese haben.
„Um mehr über die Gründe für die Herzhypertrophie der Ratten herauszufinden, suchten wir nach einem Zusammenhang zwischen dem Erbgut der Tiere und der Funktion ihrer Ribosomen. Dort findet die Translation, also die Herstellung der Proteine, statt“, sagt Ruiz-Orera. Außerdem haben die Forscher*innen untersucht, ob Fehler in der Eiweißproduktion mit der bekannten Vergrößerung der Herzen in Verbindung stehen könnten.
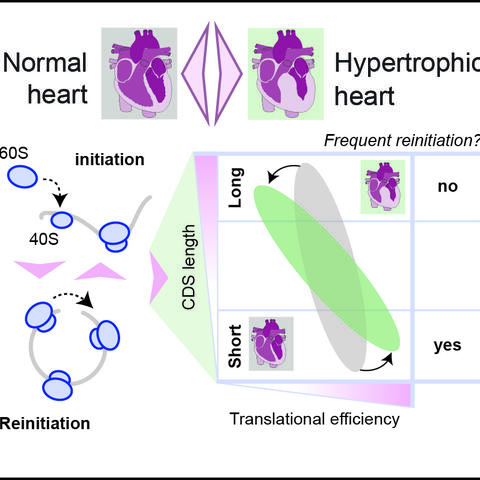
Tatsächlich stieß das Team auf eine veränderte Region im Genom der Ratten, die einen Defekt in der gesamten Proteinsynthese zu Folge hat. Allerdings wirkt sich dieser Fehler auf lange und kurze Proteine unterschiedlich stark aus. „Bei kurzen Proteinen ist der Effekt nicht so verheerend“, erläutert Ruiz-Orera. „Lange Proteine, zum Beispiel das wichtige Muskeleiweiß Titin, hingegen werden viel weniger effizient produziert.“ Man habe zeigen können, dass sich dies negativ auf den Aufbau der Sarkomere, die kleinste funktionelle Einheit der Muskelfaser, auswirke. Letztendlich führt dieser Defekt zu einer Verdickung der Herzkammern und Herzversagen.
Ähnliche Effekte sogar bei Hefezellen
„Besonders bemerkenswert ist, dass ähnliche Erbgutvariationen auch bei anderen Arten – etwa bei Mäusen, Menschen und sogar bei einzelligen Organismen wie der Hefe – die gleichen Effekte auf die Proteinsynthese haben“, berichtet Hübner. Das zeige, wie verbreitet der genetisch bedingte Defekt in den Proteinfabriken der Zellen sei, wie wenig er sich im Laufe der Evolution verändert habe und wie wichtig er für die Entstehung komplexer Krankheiten, die auch den Menschen betreffen, sei.
„Der von uns entschlüsselte Mechanismus könnte womöglich erklären, warum manche Menschen genetisch prädisponiert sind, Herzhypertrophie zu entwickeln“, sagt Hübner. „Darüber hinaus legt unsere Arbeit den Grundstein für zukünftige Studien zur genetischen Veranlagung für komplexe Krankheiten, die auch andere Organe als das Herz betreffen können.“
Text: Anke Brodmerkel
Weiterführende Informationen
- AG van Heesch am Prinses Máxima Centrum für Pädiatrische Onkologie in Utrecht
- Unbekannte Mini-Eiweiße im Herzen
Literatur
Franziska Witte, Jorge Ruiz-Orera et al. (2021): „ A trans locus causes a ribosomopathy in hypertrophic hearts that affects mRNA translation in a protein length-dependent fashion“. Genome Biology, DOI: 10.1186/s13059-021 – 02397‑w
Kontakt
Jana Schlütter
Redakteurin, Abteilung Kommunikation
Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC)
030 9406 2121
jana.schluetter@mdc-berlin.de oder presse@mdc-berlin.de
- Max-Delbrück-Centrum für Molekulare Medizin (MDC)
-
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft gehört zu den international führenden biomedizinischen Forschungszentren. Nobelpreisträger Max Delbrück, geboren in Berlin, war ein Begründer der Molekularbiologie. An den MDC-Standorten in Berlin-Buch und Mitte analysieren Forscher*innen aus rund 60 Ländern das System Mensch – die Grundlagen des Lebens von seinen kleinsten Bausteinen bis zu organübergreifenden Mechanismen. Wenn man versteht, was das dynamische Gleichgewicht in der Zelle, einem Organ oder im ganzen Körper steuert oder stört, kann man Krankheiten vorbeugen, sie früh diagnostizieren und mit passgenauen Therapien stoppen. Die Erkenntnisse der Grundlagenforschung sollen rasch Patient*innen zugutekommen. Das MDC fördert daher Ausgründungen und kooperiert in Netzwerken. Besonders eng sind die Partnerschaften mit der Charité – Universitätsmedizin Berlin im gemeinsamen Experimental and Clinical Research Center (ECRC) und dem Berlin Institute of Health (BIH) in der Charité sowie dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK). Am MDC arbeiten 1600 Menschen. Finanziert wird das 1992 gegründete MDC zu 90 Prozent vom Bund und zu 10 Prozent vom Land Berlin.