Die Evolution des Tumors
Gemeinsame Pressemitteilung von Charité und MDC
Krebszelle ist nicht gleich Krebszelle: Im erkrankten Gewebe können genetisch unterschiedliche Zellsubpopulationen in verschiedenen geografischen Regionen existieren. Diesem Phänomen der intratumoralen genetischen Heterogenität kommt in der Krebsforschung eine zunehmende Bedeutung zu. Zelluläre und molekulare Unterschiede innerhalb eines Tumors spielen bei vielen Krebserkrankungen eine wichtige Rolle, da sie sich auf die Diagnostik sowie den Einsatz von zielgerichteten Therapien auswirken können. Eine aktuelle Publikation von Charité – Universitätsmedizin Berlin, Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) und Deutschem Konsortium für Translationale Krebsforschung belegt jetzt: Dies gilt ebenso für Neuroblastome. Die bösartigen, soliden Tumore des peripheren Nervensystems sind eine relativ häufige Krebserkrankung bei Kindern. Sie entstehen meist ausgehend von Nervenzellbündeln in den Nebennieren oder entlang der Wirbelsäule und breiten sich dann im Bauchraum aus.
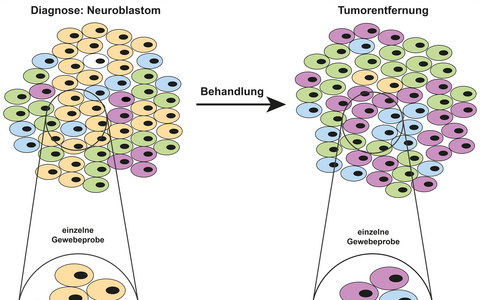
„Mit unserer Arbeit können wir zeigen, dass Erbgutveränderungen, die für das Neuroblastom typisch sind, im Verlauf der Erkrankung wieder verschwinden oder aber neu entstehen können. Diese Mutationen kommen zudem nicht gleichmäßig verteilt im Tumor vor, sondern nur in einzelnen Bereichen oder sogar nur in einzelnen Zellen eines Tumors. Sie stellen sich wie ein Mosaik dar“, fasst Dr. Karin Schmelz, Erstautorin der Studie von der Klinik für Pädiatrie mit Schwerpunkt Onkologie und Hämatologie der Charité, die zentrale Erkenntnis zusammen.
Der Tumor als Mosaik: Die Entnahme einer einzelnen Gewebeprobe eines Tumors, der sich aus genetisch unterschiedlichen Zellen zusammensetzt, birgt das Risiko der Ungenauigkeit. Möglicherweise werden nicht alle wichtigen Veränderungen der Gene erfasst. Da die Behandlung häufig den Großteil des Tumors, aber oft nicht alle Zellen absterben lässt, braucht es auch danach, bei der Tumorentfernung, eine weitere molekulare Untersuchung. Besonders beim Wiederauftreten der Erkrankung, wenn eine personalisierte, gezielte Therapie für die Patientinnen und Patienten mit Neuroblastom sehr wichtig wird, sind diese Informationen entscheidend für den Erfolg der Behandlung.
Krebs wird von evolutionären Prozessen getrieben.
„Krebs wird von evolutionären Prozessen getrieben”, sagt Dr. Roland Schwarz, Leiter der Arbeitsgruppe „Evolutionäre und Krebsgenomik“ am MDC und einer der Letztautoren. Die Zellen verändern fortlaufend ihre genetische Zusammensetzung und kämpfen ums Überleben, auch untereinander. Sie haben jeweils eigene Stammbäume, einige bilden später Metastasen oder werden schwerer behandelbar.
Die Stammbäume der Krebszellen rekonstruieren
Die Forschungsgruppe untersuchte insgesamt 140 Proben des Neuroblastoms. Diese stammten aus räumlich verschiedenen Bereichen des Tumors und wurden im Verlauf der Erkrankungen von insgesamt zehn Kindern entnommen. Das Team hat mehrere moderne Sequenzierungsmethoden an einzelnen Gewebeproben sowie computergestützte Analysen für die Auswertung genutzt.
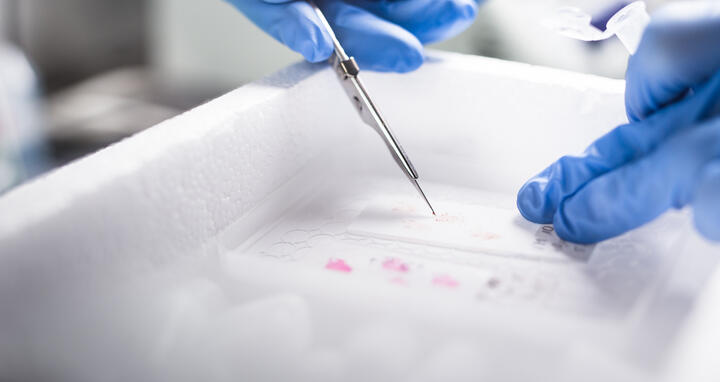
Für eine sensitive Analyse der genetischen Heterogenität haben die Forschenden nur Areale mit einem hohen Gehalt an vitalen Tumorzellen eingeschlossen. Diese wurden mit einem Skalpell aus Gewebeschnitten des gefrorenen Tumormaterials isoliert.
Die Forschenden haben die für den Verlauf und die Therapie der Erkrankung wichtigen Gene ALK, MYCN und FGFR1 besonders detailliert untersucht. Ihre Ergebnisse: ALK und MYCN waren nicht durchgehend während der Erkrankung und nicht in allen Zellen des Tumors zu finden. Veränderungen in den Genen ALK und FGFR1 können ein Angriffspunkt für eine Therapie sein, besonders wenn der Krebs erneut auftritt. Die Wissenschaftlerinnen und Wissenschaftler haben bei einigen Erkrankten festgestellt, dass ALK-Mutationen zwar bei der Diagnose, aber nicht mehr zum Zeitpunkt der chirurgischen Entfernung des Tumors auftraten. Außerdem fanden sich die Veränderungen im Gen FGFR1 nur in einzelnen Bereichen des Tumors. Darüber hinaus konnten die Forschenden eine Instabilität in der Anzahl der Genkopien der Neuroblastomzellen nachweisen. In einzelnen Fällen entwickelten sich Krebszellklone schon früh anders als der Ursprungstumor und gingen als Tochterzellen in andere Organe über, bildeten also Metastasen.
Veränderungen in der Kopienzahl bestimmter Gene in hoher räumlicher und zeitlicher Auflösung zu erfassen, ist sehr komplex.
„Veränderungen in der Kopienzahl bestimmter Gene in hoher räumlicher und zeitlicher Auflösung zu erfassen, ist sehr komplex“, erläutert der Bioinformatiker Schwarz. Seine Arbeitsgruppe – darunter der Erstautor Dr. Matt Huska vom MDC, der inzwischen am Robert Koch-Institut arbeitet – hat gemeinsam mit Teams aus Großbritannien einen Algorithmus entwickelt, der trotzdem diese Kopienzahlen höchst präzise rekonstruieren kann. Mithilfe dieses Verfahrens wiesen Schwarz und seine Kolleg*innen 2020 die kontinuierliche strukturelle Evolution in verschiedenen Krebstypen nach. „Dies konnten wir jetzt auch für das Neuroblastom belegen und detailliert zeigen, wie sich das Krebsgenom strukturell verändert“, sagt Schwarz.
Erste Hinweise für die Therapie
Professorin Angelika Eggert, Direktorin der Klinik für Pädiatrie mit Schwerpunkt Onkologie und Hämatologie und Letztautorin der Studie, erklärt: „Wir können nun besser verstehen, wie sich die Zellen des Neuroblastoms verhalten. Dieses Wissen ist essentiell für unsere Patientinnen und Patienten, die einen Rückfall der Erkrankungen erleiden, denn dann kommen oft personalisierte, gezielte Therapien zum Einsatz. Wenn sich der Tumor jedoch genetisch vielfältig präsentiert, kann eine molekular gezielte Behandlung vielleicht einen Großteil des kranken Gewebes erfassen, aber eben nicht alle Zellen. Aus den verbleibenden Zellen kann die Krebserkrankung erneut wachsen.“
Sie betont aber auch: „Unsere Ergebnisse sind weniger für die Diagnose und Therapiewahl in der Erstbehandlung relevant, denn die Diagnose eines Neuroblastoms ist durch jahrzehntelang erprobte Verfahren – etwa die Bildgebung, Urinuntersuchungen und auch mit einer einzelnen Gewebeprobe – zuverlässig möglich. Für die Behandlung in der Ersterkrankung bleibt die Chemotherapie, die auf alle schnell wachsenden Zellen gerichtet ist, das Mittel der Wahl. Wenn die Krankheit danach aber wieder auftritt, wird eine gezielte Therapie besonders wichtig. Die Therapieauswahl auf der Basis eines einzelnen Gewebestückes aus nur einer Stelle des Tumors wird wohl der genetischen Verschiedenartigkeit des Tumors nicht gerecht. Wir sollten für die Zukunft bei einem Rückfall also erwägen, das Tumorgewebe an mehreren Stellen mithilfe neuester Sequenziertechniken zu untersuchen. Das würde uns möglichst präzise Informationen über die Erkrankung liefern, um noch bessere personalisierte Therapieentscheidungen treffen zu können.“
Da dies derzeit noch mit technischen Herausforderungen verbunden ist, prüfen die Wissenschaftlerinnen und Wissenschaftler weitere methodische Möglichkeiten, darunter den Einsatz von Einzelzelltechnologien sowie Flüssigbiopsien, den Liquid Biopsies. Das sind neuartige Bluttests zur Untersuchung des Erbguts, das ein Tumor in das Blut abgibt. Anhand von mehreren Blutproben im Verlauf der Erkrankung können Veränderungen an den Genen nachgewiesen werden – ohne die Notwendigkeit einer operativ entnommenen Gewebeprobe. Beide Methoden und ihr klinischer Einsatz werden bereits intensiv an der Charité, dem Berlin Institute of Health in der Charité (BIH) und dem MDC erforscht.
Text: Charité
Weiterführende Informationen
- Pressemitteilung „Die kontinuierliche Evolution von Krebszellen“
- Klinik für Pädiatrie mit Schwerpunkt Onkologie und Hämatologie
Literatur
Karin Schmelz, Joern Toedling, Matt Huska et al. (2021): „Spatial and temporal intratumour heterogeneity has potential consequences for single biopsy-based neuroblastoma treatment decisions“. Nature Communications, DOI: 10.1038/s41467-021 – 26870‑z
Bild zum Download
Aufarbeitung des Tumorgewebes für die Sequenzierungen: Für eine sensitive Analyse der genetischen Heterogenität haben die Forschenden nur Areale mit einem hohen Gehalt an vitalen Tumorzellen eingeschlossen. Diese wurden mit einem Skalpell aus Gewebeschnitten des gefrorenen Tumormaterials isoliert.
Foto: Charité l Linda Ambrosius
Kontakte
Dr. Roland Schwarz
Leiter der Arbeitsgruppe „Evolutionäre und Krebsgenomik“
Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC)
Tel.: +49 30 9406 – 3200
Roland.Schwarz@mdc-berlin.de
Dr. Karin Schmelz
Klinik für Pädiatrie mit Schwerpunkt Onkologie und Hämatologie
Charité – Universitätsmedizin Berlin
Tel.: +49 30 450 566 132
karin.schmelz@charite.de
Jana Schlütter
Redakteurin, Abteilung Kommunikation
Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC)
Tel.: +49 30 9406 – 2121
jana.schluetter@mdc-berlin.de oder presse@mdc-berlin.de
- Max-Delbrück-Centrum für Molekulare Medizin (MDC)
-
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft gehört zu den international führenden biomedizinischen Forschungszentren. Nobelpreisträger Max Delbrück, geboren in Berlin, war ein Begründer der Molekularbiologie. An den MDC-Standorten in Berlin-Buch und Mitte analysieren Forscher*innen aus rund 60 Ländern das System Mensch – die Grundlagen des Lebens von seinen kleinsten Bausteinen bis zu organübergreifenden Mechanismen. Wenn man versteht, was das dynamische Gleichgewicht in der Zelle, einem Organ oder im ganzen Körper steuert oder stört, kann man Krankheiten vorbeugen, sie früh diagnostizieren und mit passgenauen Therapien stoppen. Die Erkenntnisse der Grundlagenforschung sollen rasch Patient*innen zugutekommen. Das MDC fördert daher Ausgründungen und kooperiert in Netzwerken. Besonders eng sind die Partnerschaften mit der Charité – Universitätsmedizin Berlin im gemeinsamen Experimental and Clinical Research Center (ECRC) und dem Berlin Institute of Health (BIH) in der Charité sowie dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK). Am MDC arbeiten 1600 Menschen. Finanziert wird das 1992 gegründete MDC zu 90 Prozent vom Bund und zu 10 Prozent vom Land Berlin.