ARHGAP36 erweitert klassische Sicht auf PKA-Regulation
Dr. Oliver Rocks wollte eigentlich gar nicht zur PKA-Regulation forschen. Als er bei einem Screening zu Proteinen, die an den Signalwegen zur Steuerung des Zellskeletts beteiligt sind, quasi über das Protein stolperte. Die Filamente des Zellskeletts werden ständig umgebaut, und die Laborgruppe von Dr. Rocks will mehr zur Steuerung dieser Änderungen herausfinden. Die Erkenntnis, dass die PKA mit diesen Signalprozessen zu tun hat, kam nicht ganz unerwartet, ungewöhnlich jedoch war die betreffende Untereinheit. „Es hat uns überrascht, die katalytische Untereinheit der PKA an der Signalsteuerung beteiligt zu sehen, denn in der Regel ist dafür die regulatorische Untereinheit zuständig“, meint Dr. Rocks.
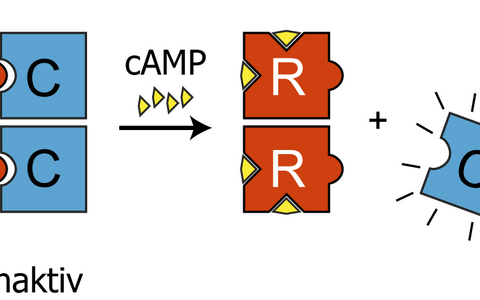
Um das Erstaunen über die katalytische Untereinheit zu verstehen, müssen wir kurz Nachwuchsbiochemikern bei der Vorlesung über die Schulter schauen. Sie zeichnen das klassische Modell der PKA-Regulation, das aussieht wie vier Legosteine – sagen wir zwei rote und zwei blaue. Die roten Steine sind die regulatorischen Untereinheiten, und ihre Aufgabe ist es, an den blauen katalytischen Untereinheiten anzudocken und diese durch die Phosphorylierung von Proteinen am Senden von Signalen zu hindern. Sie geben die katalytischen Untereinheiten nur dann frei, wenn die Zelle ein Signal erhält, das die Spiegel des chemischen Stoffs cAMP steigen lässt. cAMP kann man sich als kleine gelbe Legosteine vorstellen, die an den regulatorischen Untereinheiten andocken und diese zwingen, die blauen katalytischen Untereinheiten freizugeben.
Dieses Legosteindiagramm zeichnen Studierende der Biochemie also auf ihre Collegeblöcke. Natürlich ist das Ganze eigentlich viel komplizierter, und für verschiedene Zusammenhänge existieren jeweils weitere Regulationsebenen. Aber genau wie beim klassischen Diagramm läuft auch dort alles über die regulatorischen Untereinheiten. Nachdem also bei Dr. Rocks’ Screening überraschend die katalytischen Untereinheiten aufgetaucht waren, machten er und sein Team sich daran, herauszufinden, was da vor sich ging.
Im Screening band die katalytische Untereinheit der PKA (PKAC) an ein Protein namens ARHGAP36. Es ist ein uncharakterisiertes Protein, das heißt, man weiß kaum etwas darüber. Das GAP in ARHGAP36 steht für den Namen seiner Familie, die GTPase-aktivierenden Proteine, die bestimmte Signalwege in der Zelle regulieren.
Dr. Rebecca Eccles hat im Rahmen ihrer Promotion im Labor von Dr. Rocks untersucht, wie ARHGAP36 mit PKAC interagiert. Sie arbeitete zusammen mit anderen Wissenschaftlern vom MDC und dem Campus Buch sowie Mitarbeitenden der Universität Liverpool. Eccles entdeckte, dass ARHGAP die PKAC auf zwei Arten ausschalten kann: Entweder, indem es an sie bindet und damit blockiert, oder indem es sie auf den Weg zu einem der Recyclingzentren der Zelle schickt.
Die Aufgabe der PKA in der Zelle ist die Weiterleitung von Signalen, was die katalytische Untereinheit durch die Aktivität der Kinase erledigt – Kinasen phosphorylieren ihre Zielproteine (Substrate). ARHGAP36 hindert die PKAC, ihre Substrate zu binden, ähnlich, wie ein im Schloss steckender Schlüssel das Öffnen der Tür verhindert. Wenn wir uns die PKAC als Schloss und ihre Substrate als Schlüssel vorstellen, dann wäre ARHGAP36 – in seiner Eigenschaft als Pseudosubstrat – ein Hauptschlüssel. Es passt an das aktive Zentrum der PKAC, macht sich dort breit und hindert Substrate, an die PKAC zu binden.
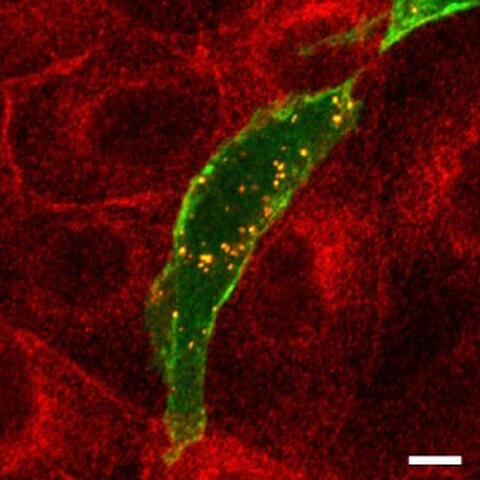
Unter dem Mikroskop: Rot fluoreszierende PKAC und grün fluoreszierendes ARHGAP36 sammeln sich zunächst in kleinen Zellbläschen (erscheinen gelb).
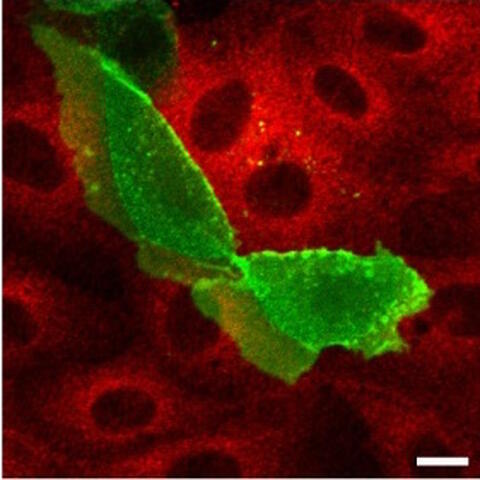
Später verschwand dann die PKAC ganz.
Bei der Betrachtung von Zellen, die rot fluoreszierende PKAC und grün fluoreszierendes ARHGAP36 exprimierten, entdeckte Dr. Eccles, dass ARHGAP36 die PKAC nicht einfach deaktivierte, sondern sie sogar ganz verschwinden ließ. Nach einigen Stunden bewegten sich die beiden Proteine gemeinsam in Zellvesikel hinein, und später verschwand dann die PKAC.
Die PKAC wurde mit Ubiquitin markiert, eine Kennzeichnung, die der Zelle mitteilt, dass ein Protein aufgespaltet werden soll. Anschließend wurde es im Endolysosom abgebaut. „Es war eine sehr starke Herunterregulation, und weil sich bei PKAC um ein zytosolisches Protein handelt, waren wir überrascht, dass es über den endolysosomalen Weg abgebaut wurde“, so Eccles. Die meisten zytosolischen Proteine werden durch einen zellulären Recyclingmechanismus namens Proteosom zerlegt, während das Endolysosom normalerweise Membranproteine aufschließt.
Da die PKA in verschiedenen Geweben vorkommt, wollten die Forscher wissen, wo und wann sie durch ARHGAP36 gehemmt wird. „ARHGAP36 ist ein starker Inhibitor, es ist also wichtig, dass es die PKA nicht einfach überall ausschaltet“, erklärt Rocks. Sie fanden heraus, dass ARHGAP36 nicht ständig in sämtlichen Zellen vorhanden ist – seine Expression ist vielmehr recht eingeschränkt.„Es wird während der Muskelentwicklung beim Embryo aktiviert, vielleicht, weil es hierbei wichtig ist, die PKA unter Kontrolle zu halten.” Eine Hochregulation von ARHGAP36 findet sich auch bei mindestens einem der vier Subtypen des Medulloblastoms, der am meisten verbreiteten Art von Hirntumoren bei Kindern. „Aus Sicht des Tumors ist vielleicht eine strenge Regulation entscheidend, damit die PKA dort, wo sie gebraucht wird, nicht deaktiviert wird“, meint Rocks. Andere Forscher berichteten kürzlich, dass Änderungen im PKA-Signalsystem bei vielen Krebsarten das Tumorwachstum beeinflussen könnten.
Die Erkenntnis, dass ein so gut erforschtes Protein wie die PKA auf unbekannte Weise reguliert werden kann, ist sehr interessant. Die genaue biologische Rolle von ARHGAP36 bleibt noch zu entdecken, aber es kann gut sein, dass es an der Muskelentwicklung und bei manchen Krebsarten am Tumorwachstum beteiligt ist. Das Verständnis der Regulation von Signalwegen könnte zukünftig auch bei der Medikamentenentwicklung von Nutzen sein, denn auf Signalwege abzielende Wirkstoffe bieten oft Möglichkeiten zur Blockierung von Enzymen, die sonst schwer manipulierbar sind. In jedem Fall haben die Untersuchungen zu ARHGAP36 im Labor Rocks das klassische Legomodell der PKA-Regulation nun komplexer gemacht.
Rebecca L. Eccles1, Maciej T. Czajkowski1,2,Carolin Barth1, Paul Markus Müller1, Erik McShane1, Stephan Grunwald1, Patrick Beaudette1, Nora Mecklenburg1, Rudolf Volkmer4, Kerstin Zühlke1, Gunnar Dittmar1, Matthias Selbach1, Annette Hammes1, Oliver Daumke1,5, Enno Klussmann1,6, Sylvie Urbé3, Oliver Rocks1 (2016): „Bimodal antagonism of PKA signalling by ARHGAP3.“ Nature Communications. doi:10.1038/NCOMMS12963
1Max-Delbrück-Center für Molekulare Medizin in der Helmholtz-Gemeinschaft, Berlin; 2Berlin Institute of Health (BIH), Berlin; 3Cellular and Molecular Physiology, Institute of Translational Medicine, University of Liverpool, Liverpool, Vereinigtes Königreich; 4Leibniz-Institut für Molekulare Pharmakologie, Berlin; 5Institut für Chemie und Biochemie, Freie Universität Berlin, Berlin; 6DZHK, Deutsches Zentrum für Herz-Kreislaufforschung, Berlin
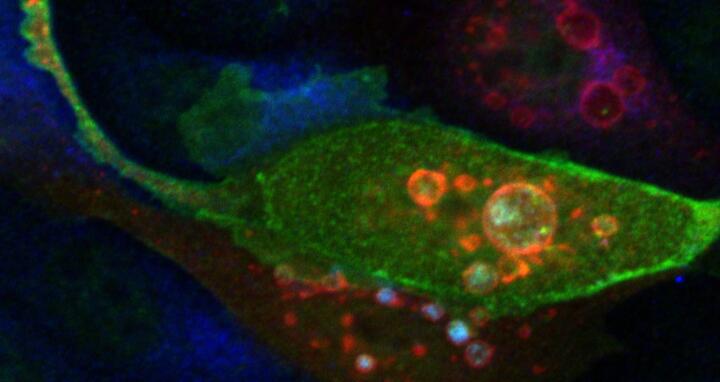
Beitragsbild: PKAC, blau fluoreszierend, sammelt sich in roten, vergrößerten Vesikelbläschen, sobald ARHGAP36 (grün) in der Zelle vorliegt. Bild: Rebecca Eccles, MDC.