Wie Zellen sich selbst verschlingen
Sascha Martens und er seien schon immer ein „Super-Team“ gewesen, sagt Oliver Daumke und strahlt. Er erinnere sich gern an die Zeit, zu der die beiden Männer gemeinsam studierten, dann während der Diplomarbeit die Arbeitsbank teilten und später für ihren Postdoc Seite an Seite im selben Labor in Cambridge standen. „Unsere Zusammenarbeit hat immer wunderbar funktioniert.“
Bis heute hat sich daran nichts geändert, obwohl die Freunde inzwischen in unterschiedlichen Städten Europas arbeiten, etwa acht Autobahnstunden voneinander entfernt. Denn während Daumke 2007 von England nach Berlin zog, um als Strukturbiologe am MDC zu arbeiten, verschlug es Martens an die Universität Wien. Dort erforscht er seitdem die zelluläre Autophagie (griechisch für „sich selbst verzehrend“). Denn wenn Zellen Bestandteile von sich selbst beseitigen und sie zu wertvollen Nährstoffen recyclen wollen, verspeisen sie sie in einem komplexen Prozess, über den immer noch nicht alles bekannt ist.
Wo die Zelle abbeißt
Woher weiß die Zelle so genau, wo sie abbeißen soll? Das war lange ein Rätsel.
„Woher weiß die Zelle so genau, wo sie abbeißen soll? Das war lange ein Rätsel“, sagt Daumke. Zusammen mit James Hurley von der University of California in Berkeley konnten die Wissenschaftler diese Frage nun beantworten und beschreiben ihre Ergebnisse im Fachblatt „Molecular Cell“.
„Autophagie ist ein grundlegender Prozess in der Biologie“, sagt Daumke. Wenn er nicht richtig funktioniert, verursacht das Krankheiten. Im Nervensystem bilden sich dann schädliche Ablagerungen und es komme zu Demenz. Krebszellen nutzen die Autophagie andererseits, um schnell Energie und Baumaterial für ihr zerstörerisches Wachstum zu gewinnen. „Wer Autophagie im Detail versteht, kann sie auch steuern“, sagt Daumke – und auf diese Weise in der Zukunft möglicherweise Krankheiten behandeln.
Zahlreiche Proteine helfen
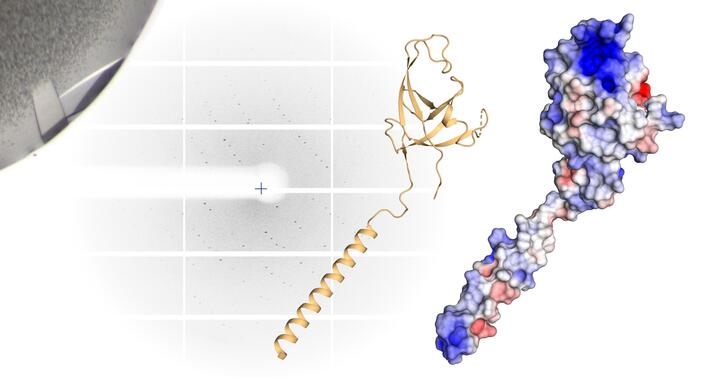
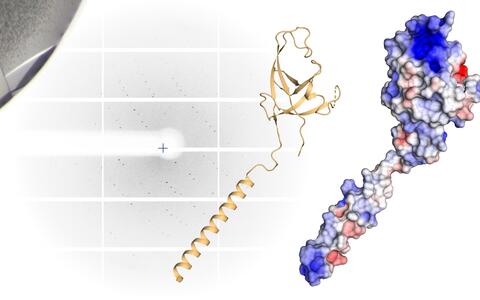
Wichtig für die Autophagie: In einer vereinfachten dreidimensionalen Darstellung der „Klaue“ sind Arm und Hand gut zu erkennen (links). Im raumfüllenden Molekülmodell (rechts) sind positive Ladungen rot, negative Ladungen blau – der stark geladene Fleck an der Spitze des Moleküls sticht dabei besonders heraus.
Im Inneren der Zelle kommen für diesen Vorgang zahlreiche Moleküle zusammen. Moleküle wie das Protein p62 legen sich etwa auf kaputte, verklumpte Eiweiße und machen sie damit für die Zelle unwiderstehlich. Diese stülpt anschließend eine Membran über ihr „Essen“, umschließt es wie mit einem Mund. Verdauungsenzyme zerkauen dann alles, was sich darin befindet.
Martens hat sich schon seit Jahren den Kopf darüber zerbrochen, wie genau die Anfangsphase der Autophagie abläuft, was also den zellulären Appetit auslöst. Wenn die Freunde telefonierten oder sich trafen, haben sie immer wieder darüber diskutiert, sagt Daumke. „Sascha hat das Thema einfach nicht losgelassen.“
Eines Tages entdeckte Martens Gruppe Indizien dafür, dass das p62-Protein auf der einen Seite die zu verdauenden Proteine erkennt, auf der anderen Seite aber auch in direkten Kontakt mit dem Beißapparat der Zelle tritt und damit als Adapter fungiert. Doch für genauere Untersuchungen fehlte ihm die Ausrüstung. „Sascha wollte wissen, was auf der molekularen Ebene passiert – und da hat er mich angesprochen“, sagt Daumke.
Eine molekulare Hand
Daumke und sein Team sind Spezialisten fürs Kleinste und können Molekülen sogar auf die Atome schauen. Im Labor stellen sie Proteine in großen Mengen her, züchten daraus Kristalle und beschießen diese mit einem intensiven Röntgenstrahl. Der Strahl bricht sich im Kristall und aus dem für jedes Protein einzigartigen Muster können die Forscher errechnen, wie die Proteine aufgebaut sind. Dabei einstehen detaillierte Modelle, genauer als ein Mikroskop sie je darstellen könnte.
Marie Witt, Oliver Daumke und Tobias Bock-Bierbaum
Die Doktorandin Marie Witt und der Postdoktorand Tobias Bock-Bierbaum aus Daumkes Labor schauten sich das p62-Molekül und die Bestandteile des Autophagie-Apparates genauer an. Sie entdeckten eine ungewöhnliche Struktur an einem Ende des FIP200-Proteins, welche für die Autophagie essenziell ist. „Wir haben eine Art Arm, Hand und fingerartigen Fortsätze gefunden und haben das Ganze Klaue genannt“, sagt Marie Witt.
Das Innere der Klaue sei elektrostatisch stark positiv geladen, sagt die Wissenschaftlerin: „So etwas macht uns Strukturbiologen immer stutzig.“ Denn positive und negative Ladungen an den Proteinbausteinen ziehen sich gegenseitig an. „Wir haben uns gefragt: Vielleicht bindet dort das p62?“
Ein fester Griff verbindet
Mit diesen Befunden wandte sich Daumke wieder an seinen Studienfreund. Den Verdacht erhärteten die Wissenschaftlerinnen und Wissenschaftler in Wien und Berlin durch weitere Versuche: „Die Klaue von FIP200 packt das p62 und hält es fest“, sagt Bock-Bierbaum. Durch gezielte Mutationen veränderten die Wissenschaftler die elektrostatische Ladung der Hand. Der feste Griff lockerte sich. „Wir sind daher überzeugt, die Bindestelle identifiziert zu haben“, sagt Witt.
Martens Team wies daraufhin nach, dass p62 und die Klaue von FIP200 auch in lebenden menschlichen Zellen zusammen vorkommen. Entfernte Martens die Klaue aus dem FIP200 Protein, nahm der Appetit der Zelle auf mit p62-markierte Leckerbissen ab und die Autophagie wurde gebremst.
Offene Fragen
„Damit hatten wir die Verbindung zwischen der zu verdauenden Fracht einerseits und der Autophagie-Maschinerie anderseits nachgewiesen“, sagt Witt. „Dass wir diesen Link gefunden haben, ist sehr wichtig für die Autophagie-Forschung“, ergänzt Daumke. „Nun können wir rekonstruieren, wann welche Komponente aktiv wird. Das ist eine richtige schöne Signalkaskade.“
Wissenschaft bedeutet immer, dass man etwas gerne macht, und das mit Leuten, mit denen man gern zusammenarbeitet.
Trotzdem seien einige Fragen noch unbeantwortet, sagt Daumke. „Am liebsten hätten wir eine Struktur des Komplex aus p62 und FIP200“. In ihren Experimenten hätten sie beobachtet, dass FIP200 nur sehr schwach an seinen Adapter bindet. „Das macht die Sache interessant, aber auch schwierig zu untersuchen.“
Es gibt also genügend Stoff für weitere Kooperation mit Sascha Martens Labor in Wien. Doch daran mangele es ohnehin nicht, sagt Daumke. „Durch unsere lange Freundschaft machen wir einfach das, was uns Spaß macht und untersuchen, was uns interessiert“, sagt Daumke. „Wissenschaft bedeutet immer, dass man etwas gerne macht, und das mit Leuten, mit denen man gern zusammenarbeitet.“
Text: Martin Ballaschk
Literatur
Eleonora Turco et al. (2019): „FIP200 claw domain binding to p62 promotes autophagosome formation at ubiquitin condensates“. Molecular Cell, Vol 74, 2. DOI:10.1016/j.molcel.2019.01.035