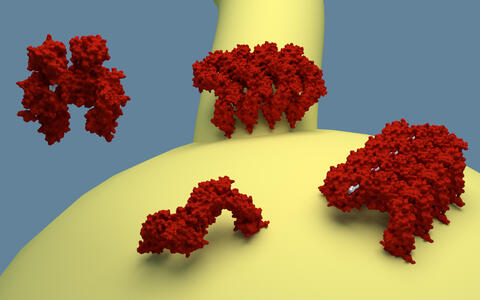
Wie Proteine Zellmembranen verformen
Auf dem Jahrmarkt zaubern Künstler mit ein paar Handgriffen aus einfachen Ballons kunstvolle Figuren. Dafür verformen sie die Ballonhaut und schnüren Teile davon ab. Auf ähnliche Art erzeugen Zellen in ihrer Außenhaut (Zellmembran) kleine Bläschen (Vesikel), die sie in ihr Inneres transportieren. Vesikel dienen zur Aufnahme von Nährstoffen und sind wichtig für die Weiterleitung von Nervensignalen.
Molekulare Maschinen verformen die Membran
EHD-Proteine sind an der Bildung solcher Vesikel beteiligt. Sie binden von innen an die Zellmembran und bilden dort lange Ketten und Ringe. Diese Ringe stülpen die Membran ein, ziehen sie zusammen und trennen sie letztlich von der Außenhaut der Zelle ab.
Oliver Daumke vom Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) erforscht die räumliche Struktur und die Funktionsweise der EHD-Proteine. In einer früheren Studie analysierten er und sein Team bereits die 3D-Struktur einer inaktiven EHD-Form, die nicht an die Membran gebunden ist. Wie EHD-Proteine aktiviert werden, um an Membranen zu binden und diese zu röhrenförmigen Gebilden zu verformen, war bisher nicht bekannt.
Das Protein klappt auf und gibt spezialisierte Regionen frei
Die aktive Form der molekularen EHD-Maschine, wie sie im Kontakt mit der Membran vorkommt, beschreiben Daumke und sein Doktorand Arthur Alves de Melo zusammen mit internationalen Kollegen in der aktuellen Ausgabe der Fachzeitschrift PNAS. Der Vergleich der aktiven mit der inaktiven Proteinstruktur ergab, dass die EHD-Moleküle beim Binden an die Membran aufklappen. Dabei legen sie Regionen frei, die die es ihnen erlauben, sich zu ausgedehnten Ketten und Ringen zusammenzulagern. Ein weiterer spezialisierter Bereich dreht sich dabei so, dass er direkt mit der Membran Kontakt aufnehmen kann und die Proteine dort verankert.
Damit hat Daumkes Team zwei Schritte in der Arbeitsweise von EHD beschrieben. „Um den kompletten Arbeitszyklus und damit die Funktionsweise der molekularen EHD-Maschinen zu verstehen, müssen wir noch verschiedene andere Zustände analysieren“, sagt er. „Das ist eine Aufgabe für die nächsten Jahre.“
Text: Martin Ballaschk
Arthur Alves Melo1,2, Balachandra G. Hegde3, Claudio Shah1,2, Elin Larsson4, J. Mario Isas5, Séverine Kunz1, Richard Lundmark4,6, Ralf Langen5, and Oliver Daumke1,2 (2017): „Structural insights into the activation mechanism of dynamin-like Eps15-homology domain proteins.“ PNAS. doi:10.1073/pnas.1614075114
1Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft, Berlin; 2Institut für Chemie und Biochemie, Freie Universität Berlin; 3Department of Physics, Rani Channamma University, Karnataka, Indien; 4Medical Biochemistry and Biophysics, Universität Umeå, Schweden; 5Zilkha Neurogenetic Institute, University of Southern California, Los Angeles, USA; 6Integrative Medical Biology, Universität Umeå, Schweden.