Das Immunsystem mischt überall mit
Immunzellen sind überall im Körper. „Früher dachte man, dass zumindest das Gehirn eine Art No-Go-Zone für das Immunsystem darstellt“, sagt Professor Klaus Rajewsky, der Leiter der Arbeitsgruppe „Immunregulation und Krebs“ am Max-Delbrück-Centrum für Molekulare Medizin (MDC). Doch das hat sich als folgenschwerer Irrtum erwiesen. „Alle wichtigen Erkrankungen des Zentralen Nervensystems wie Alzheimer oder Parkinson haben eine starke immunologische Komponente“, betont Rajewsky. „Und inzwischen gehen wir sogar davon aus, dass es kaum eine Krankheit des Menschen gibt, an der das Immunsystem nicht beteiligt ist.“
Auch aus diesem Grund wenden sich immer mehr Wissenschaftlerinnen und Wissenschaftler der Immunologie zu. „Es ist ein hochexplosives Forschungsfeld“, sagt Rajewsky, der auch dem Leitungsgremium der Helmholtz-Initiative Immunology & Inflammation, kurz I&I, angehört. Für dieses Projekt haben sich seit dem Jahr 2017 insgesamt 23 Arbeitsgruppen aus den fünf Helmholtz-Zentren in Berlin, Bonn, Hannover, Heidelberg und München zusammengeschlossen. Gemeinsam wollen sie aktuelle, perspektivisch wichtige Fragen der Immunologie beantworten. Er sei sich sicher, dass Immuntherapien die Medizin in den kommenden zehn Jahren dramatisch verändern werden, sagt Rajewsky.
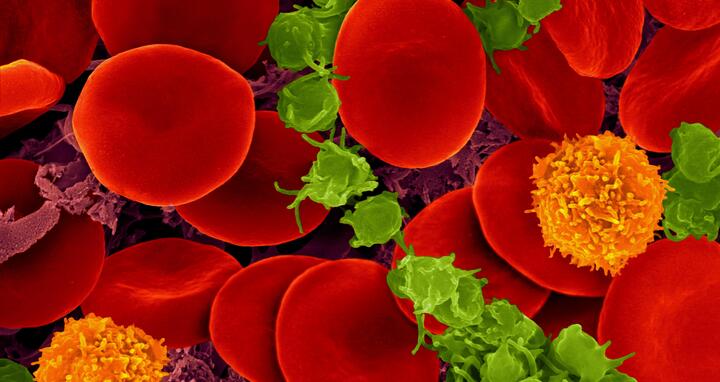
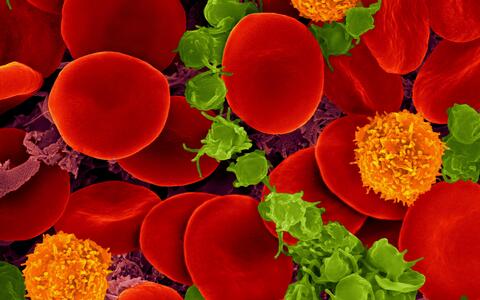
Menschliches Blut mit roten Blutkörperchen, T-Zellen (orange) und Blutplättchen (grün)
Defekte T-Zellen von Kindern sollen repariert werden
Um sich über die neuesten Entwicklungen auf dem Forschungsgebiet auszutauschen, hatten die Deutsche Gesellschaft für Immunologie (DGfI) und die Italienische Gesellschaft für Immunologie, klinische Immunologie und Allergologie SIICA Mitte September zu einer viertägigen Konferenz nach München eingeladen. Im Rahmen dieser Tagung hatten Professorin Ellen Renner vom Helmholtz Zentrum München und Professor Tim Niehues, Chefarzt des Zentrums für Kinder- und Jugendmedizin am Helios Klinikum Krefeld, in Abstimmung mit Rajewsky ein Satellitensymposium der I&I Initiative organisiert.
„Wir hatten tolle Vortragende und bestimmt 200 Besucherinnen und Besucher, eher mehr“, sagt Rajewsky. Er selbst berichtete auf dem Symposium von seinen Versuchen, Kindern zu helfen, die unter angeborenen Defekten der T-Zellen leiden. Ihren Immunzellen gelingt es beispielsweise nicht, gegen das verbreitete Epstein-Barr-Virus vorzugehen. Infizieren sich diese Kinder damit, kommt es zu lebensbedrohlichen Erkrankungen – weshalb die meisten der kleinen Patienten früh versterben.
„Unsere Idee ist es, den Gendefekt entweder in den T-Zellen selbst oder in den hämatopoetischen Stammzellen, aus denen die T-Zellen hervorgehen, per Gen-Editierung zu beheben“, erläutert Rajewsky. Dazu benutzen der Forscher und sein Team die als Genschere bekannt gewordene CRISPR/Cas9-Methode. „Die Ergebnisse, die wir bislang im Mausmodell und mit isolierten menschlichen T-Zellen erzielt haben, sind sehr ermutigend“, sagt der Immunologe.
Gezielte Hilfe für ein stillgelegtes Immunsystem
Über eine Manipulierung von T-Zellen berichtete auf dem Symposium auch Professor Dirk Busch vom Institut für Medizinische Mikrobiologie, Immunologie und Hygiene der Technischen Universität München (TUM). Die Methode, die Busch und sein Team gerade erarbeiten, ist für Patienten gedacht, deren eigenes Immunsystem vorübergehend außer Gefecht gesetzt wurde - zum Beispiel durch eine Knochenmarkstransplantation im Rahmen einer Tumorbehandlung.
In der Zeit, in der sich das blutbildende System erst einmal wieder neu aufbauen muss, sind die Patienten besonders anfällig für Infektionen. Buschs Idee ist es, ihnen in dieser Phase modifizierte, im Idealfall patienteneigene T-Zellen zu verabreichen, die zuvor per Gen-Editierung einen neuen Rezeptor erhalten haben. Dieser ist zum Beispiel speziell auf Cytomegaloviren (CMV) ausgerichtet. CMV sind ebenfalls sehr verbreitete Viren, die bei gesunden Menschen normalerweise keine Symptome hervorrufen. Patienten mit einem geschwächten Immunsystem können durch sie jedoch lebensgefährliche Erkrankungen erleiden.
Wie Busch berichtete, kann die Gabe von sehr wenigen modifizierten T-Zellen – im Extremfall sogar von einer einzigen Zelle - aufgrund deren rascher Vermehrung ausreichen, um CMV-Infektionen bei immungeschwächten Patienten wirkungsvoll zu bekämpfen. Der Forscher verfügt inzwischen über eine ganze Bibliothek von Rezeptoren, die auf verschiedene klinisch relevante Viren gerichtet sind. Derzeit werde das Verfahren seines Kollegen noch im Rahmen klinischer Studien erprobt, sagt Rajewsky. Aber er sei sich sicher, dass es schon in absehbarer Zeit breite Anwendung finden werde.
Grundlagenforscher und Kliniker konnten sich austauschen
Professor Eicke Latz vom Deutschen Zentrum für Neurodegenerative Erkrankungen (DZNE) in Bonn und Direktor am Institut für Angeborene Immunität der Universität Bonn sprach auf dem Symposium über den Einfluss der Ernährung auf entzündliche Prozesse im Körper. Latz hat einen wichtigen Stoffwechselweg entdeckt, über den die hierzulande übliche fett- und eiweißreiche Diät die myeloischen Zellen des Immunsystems so beeinflusst, dass sie entzündliche Erkrankungen vorantreiben können. Daraus ergeben sich neue prophylaktische und therapeutische Perspektiven.
Auch Professor Hans-Reimer Rodewald vom Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg hielt auf dem Symposium der I&I Initiative einen Vortrag. Er berichtete, wie sich verschiedene Immunzellen im Körper aus Stammzellen entwickeln, um ein funktionsfähiges Immunsystem zu bilden und – beispielsweise nach einem größeren Blutverlust – zu erhalten. In seinen jüngsten Arbeiten ist es Rodewald gelungen, Zellen des Immunsystems mit einem Barcode-System auszustatten und so ihren Weg im lebenden Organismus zu verfolgen. Auf diese Weise lässt sich untersuchen, wie die Vielzahl verschiedener Zelltypen im Blut entsteht.
„Zusammenfassend – und ohne auf alle Beiträge hier eingehen zu können – lässt sich sagen, dass die Teilnehmer an unserem Symposium am Ende sehr zufrieden waren“, sagt Rajewsky. „Es hat grundlagenorientierte Forscher mit Klinikern zusammengebracht und zwischen allen kam es zu einem nützlichen und angenehmen Austausch.“
Robin Graf
Der Otto-Westphal-Promotionspreis an Robin Graf vom MDC
Grund zur Freude hatte Rajewsky auf der DGfI-Konferenz auch noch aus einem anderen Grund: Gleich zwei Forschende des MDC wurden in München mit begehrten Preisen ausgezeichnet. Der mit 1.500 Euro dotierte Otto-Westphal-Promotionspreis ging an Dr. Robin Graf aus der Arbeitsgruppe von Rajewsky. In seiner herausragenden Dissertation habe Graf die Relevanz des B-Zell-Rezeptors in der Entwicklung der B1-Zellen untersucht, hieß es in der Begründung der Jury.
B-Zellen, die zu den weißen Blutkörperchen, den Lymphozyten, gehören, sind als einzige Zellen des Immunsystems in der Lage, Antikörper zu bilden. Mit seiner wichtigsten Studie, die im Februar dieses Jahres im Fachblatt Science veröffentlicht wurde, konnte Graf gemeinsam mit weiteren Forschern und Forscherinnen aus der Gruppe von Rajewsky aufzeigen, dass der B-Zell-Rezeptor eine instruktive Rolle in der Entwicklung der B1-Zellen spielt. Den B1-Zellen wird eine wichtige Funktion bei der natürlichen Immunität von Neugeborenen, also dem angeborenen Immunsystem, zugeschrieben. B2-Zellen hingegen sind vor allem für die erworbene Körperabwehr zuständig.
Dr. Kathrin de la Rosa
Auch die MDC-Forscherin Kathrin de la Rosa wurde ausgezeichnet
Dr. Kathrin de la Rosa (geborene Pieper), die seit Juli 2018 am MDC die Arbeitsgruppe „Immunmechanismen und humane Antikörper“ leitet, erhielt den ebenfalls mit 1.500 Euro dotierten Fritz-und-Ursula-Melchers-Postdoktorandenpreis. Die Forscherin hatte als Postdoktorandin im Labor von Professor Antonio Lanzavecchia an der Eidgenössischen Technischen Hochschule (ETH) Zürich mit zwei Veröffentlichungen in der Fachzeitschrift Nature einen neuen und völlig unerwarteten molekularen Mechanismus der Antikörper-Vielfalt beschrieben.
Gemeinsam mit ihrem Team entdeckte de la Rosa einen Antikörper, der eine besondere Eigenschaft aufweist: Er „stiehlt“ sich ein Segment von einem Gen der B-Zelle namens LAIR1. Dieses liegt auf einem Chromosom, das eigentlich gar keine Bauanleitungen für Antikörper enthält. Durch diesen Trick verfügt der Antikörper über eine Extra-Domäne, mit deren Hilfe er verschiedene Varianten des Malaria-Erregers Plasmodium falciparum erkennen kann. Er sei somit, so begründete die Jury ihre Wahl, ein neues Instrument zur Bekämpfung der Malaria und ein erfolgversprechender Kandidat für die Entwicklung eines Impfstoffs.
Text: Anke Brodmerkel
Weiterführende Informationen
- Zukunftsthema Immunologie und Inflammation (I&I)
- Pressemitteilung der Deutschen Gesellschaft für Immunologie: Ausgezeichnet!