Was Statine mit den Muskeln machen
Weltweit nehmen rund 20 Millionen Menschen Statine ein. Allein in Deutschland sind es fast fünf Millionen. Die Medikamente werden zur Senkung des Cholesterinspiegels verordnet, um Folgeerkrankungen wie Herzinfarkt oder Schlaganfall vorzubeugen. „Statine sind allerdings mit einer Reihe von Nebenwirkungen verbunden, weshalb viele Patientinnen und Patienten sie nicht zuverlässig einnehmen“, sagt Professorin Simone Spuler, die Leiterin der MDC-Arbeitsgruppe Myologie und der Muscle Research Unit am ECRC (Experimental and Clinical Research Center), einer gemeinsamen Einrichtung des MDC und der Berliner Charité – Universitätsmedizin Berlin.
Zu den häufigsten unerwünschten Begleiterscheinungen der Statine gehören Muskelkrämpfe und –schmerzen. „Angesichts der Nutzen von Statinen für die Gesundheit der westlichen Weltbevölkerung werden diese Nebenwirkungen jedoch oft als vernachlässigbar eingestuft“, sagt Spuler. Sie und ihr Team wollten es genauer wissen und herausfinden, was Statine konkret in den Muskelzellen auslösen. Zu diesem Zweck initiierten sie – allein mit DFG-Geldern und ohne Unterstützung der Pharmaindustrie – eine Studie, die jetzt im Fachblatt „Scientific Reports“ erschienen ist.
Statine störten die Produktion von mehr als 900 Proteinen
Ganz offensichtlich üben Statine in der allgemein üblichen Wirkstoffmenge dramatische strukturelle, funktionelle und metabolische Effekte auf die Muskeln aus.
Für ihre Untersuchung setzte die Gruppe um die Erstautorin der Studie, Dr. Stefanie Anke Grunwald von der Muscle Research Unit am ECRC, insgesamt 22 Populationen menschlicher Skelettmuskelzellen jeweils zwei verschiedenen Statinen aus: zum einem dem fettlöslichen Wirkstoff Simvastatin, zum anderen dem wasserlöslichen Wirkstoff Rosuvastatin. Anschließend untersuchten die Forscherinnen und Forscher, welche Gene in den Zellen jeweils angeschaltet waren und in Proteine umgesetzt wurden und welche nicht. Zudem analysierten sie den Stoffwechsel der Zellen und beurteilten ihren Zustand anhand morphologischer Kriterien.
„Aufgabe der Statine ist es, ein bestimmtes Enzym bei der Cholesterinbildung zu blockieren, das HMG-CoA“, erklärt Grunwald. Es habe in der Vergangenheit einige Studien gegeben, die die Auswirkungen von Statinen auf den menschlichen Muskel beleuchten wollten. „Viele von ihnen fanden jedoch weder mit Muskelzellen noch mit menschlichen Zellen statt“, sagt Grunwald Die Ausschaltung eines zentralen Enzyms habe komplexe Folgen – die sie und ihre Kolleginnen und Kollegen nun auch mit modernsten Computer-Modelling-Methoden beleuchtet haben.
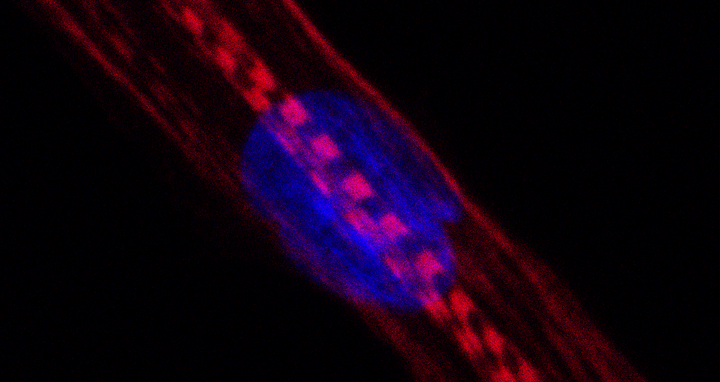
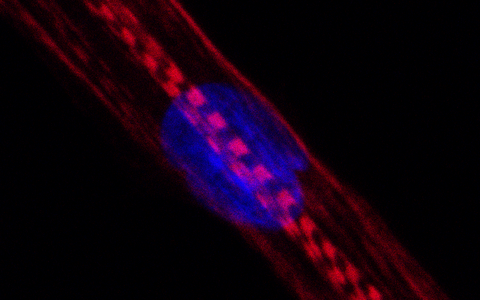
Humane Muskelzelle. Bei Menschen, die Statine nehmen, war unter anderem die Produktion von Myosinen gestört. Diese Proteine sind im Bild rot angefärbt, der Zellkern blau. Die Querstreifen zeigen, dass die Zelle sich in eine reife Muskelfaser entwickelt.
„Die Ergebnisse waren hochinteressant“, sagt Spuler. „Ganz offensichtlich üben Statine in der allgemein üblichen Wirkstoffmenge dramatische strukturelle, funktionelle und metabolische Effekte auf die Muskeln aus.“ Sie und ihr Team stießen in den untersuchten Zellen beispielsweise auf rund 2.500 Gene, die in Anwesenheit der Medikamente anders reguliert wurden als gewöhnlich. Dadurch war die Produktion von mehr als 900 Proteinen verändert: Sie wurden entweder in zu geringen oder zu großen Mengen hergestellt. Der Einfluss von Simvastatin war diesbezüglich höher als der von Rosuvastatin.
Die Zellen wuchsen nicht wie gewohnt
Beide Statine drosselten in den Muskelzellen nicht nur die Biosynthese von Cholesterin, sondern auch den Fettsäure-Stoffwechsel insgesamt sowie die Produktion von Eicosanoiden. Dabei handelt es sich um eine Gruppe hormonähnlicher Substanzen, die aus mehrfach ungesättigten Fettsäuren hervorgehen. Sie wirken sowohl innerhalb als auch außerhalb von Zellen als Signalmoleküle und sind in zahlreiche biologische Wirkmechanismen eingebunden. Unter anderen sind sie an der Entwicklung differenzierter Muskelzellen aus Muskelvorläuferzellen beteiligt. „Und sie sind auch in die Schmerzentstehung involviert. Das war für uns ein wichtiger Anhaltspunkt, dass wir hier auf der richtigen Spur sind“, sagt Grunwald.
„Mithilfe funktioneller Analysen konnten wir bestätigen, dass die Entwicklung, das Wachstum und die Teilung der Skelettmuskelzellen durch die Statine beeinträchtigt werden“, sagt Spuler. Sie und ihr Team fanden einen Weg, um die negativen Effekte der Medikamente etwas einzudämmen: „Die Gabe von Omega-3- oder Omega-6-Fettsäuren machte die Wirkungen von Simvastatin und Rosuvastatin teilweise rückgängig“, berichtet die Wissenschaftlerin. Eine ergänzende Einnahme derartiger Präparate könne daher eine Möglichkeit sein, um einer Statin-Myopathie vorzubeugen oder sie zu behandeln.
Statine sind keine Life-Style-Pillen
Unsere Erkenntnisse sollten dazu führen, dass die Gabe von Statinen künftig sehr viel kritischer gesehen werden sollte, als es momentan der Fall ist.
„Dennoch sollten unsere Erkenntnisse meines Erachtens dazu führen, dass die Gabe von Statinen künftig sehr viel kritischer gesehen werden sollte, als es momentan der Fall ist“, sagt Spuler. In vielen westlichen Ländern der Welt hätten sich die Cholesterinsenker fast schon zu einem Life-Style-Präparat entwickelt. „Das ist keinesfalls ein positiver Trend“, sagt Spuler. Ihrer Ansicht nach sollten Ärzt*innen und Patient*innen sollten in jedem individuellen Fall den Nutzen und die möglichen Gefahren der Medikamente gut abwägen.
Text: Anke Brodmerkel
Weiterführende Informationen
Nachrichten zur Muskel-Forschung des MDC
Literatur
Grunwald, Stefanie Anke et al. (2020): „Statin-induced myopathic changes in primary human muscle cells and reversal by a prostaglandin F2 alpha analogue”, Scientific Reports, DOI: 10.1038/s41598-020 – 58668‑2.
Bild zum Download
Humane Muskelzelle. Bei Menschen, die Statine nehmen, war unter anderem die Produktion von Myosinen gestört. Diese Proteine sind im Bild rot angefärbt, der Zellkern blau. Die Querstreifen zeigen, dass die Zelle sich in eine reife Muskelfaser entwickelt.
Foto: Andreas Marg, MDC.
Kontakte
Prof. Dr. Simone Spuler
Experimental and Clinical Research Center (ECRC)
Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) und Charité – Universitätsmedizin Berlin
Leiterin der Arbeitsgruppe „Myologie“
+49 30 450 5405 01 oder +49 30 450 5405 04
simone.spuler@mdc-berlin.de oder simone.spuler@charite.de
Jana Schlütter
Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC)
Redakteurin, Abteilung Kommunikation
+49 – 30 9406 2121
jana.schluetter@mdc-berlin.de oder presse@mdc-berlin.de
- Das Max-Delbrück-Centrum für Molekulare Medizin (MDC)
-
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft gehört zu den international führenden biomedizinischen Forschungszentren. Nobelpreisträger Max Delbrück, geboren in Berlin, war ein Begründer der Molekularbiologie. An den MDC-Standorten in Berlin-Buch und Mitte analysieren Forscher*innen aus rund 60 Ländern das System Mensch – die Grundlagen des Lebens von seinen kleinsten Bausteinen bis zu organübergreifenden Mechanismen. Wenn man versteht, was das dynamische Gleichgewicht in der Zelle, einem Organ oder im ganzen Körper steuert oder stört, kann man Krankheiten vorbeugen, sie früh diagnostizieren und mit passgenauen Therapien stoppen. Die Erkenntnisse der Grundlagenforschung sollen rasch Patient*innen zugutekommen. Das MDC fördert daher Ausgründungen und kooperiert in Netzwerken. Besonders eng sind die Partnerschaften mit der Charité – Universitätsmedizin Berlin im gemeinsamen Experimental and Clinical Research Center (ECRC) und dem Berlin Institute of Health (BIH) in der Charité sowie dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK). Am MDC arbeiten 1600 Menschen. Finanziert wird das 1992 gegründete MDC zu 90 Prozent vom Bund und zu 10 Prozent vom Land Berlin.