4,6 Millionen Euro für neuartige CAR-T-Zelltherapie
Gemeinsame Pressemitteilung des Max Delbrück Center und der Charité – Universitätsmedizin Berlin
CAR-T-Zelltherapien sind oft der letzte Ausweg für Patient*innen mit bestimmten Formen von Blut- oder Lymphdrüsenkrebs, die auf gängige Behandlungen nicht ansprechen. Dabei werden Immunzellen (T‑Zellen) der Erkrankten im Labor mit einem chimären Antigenrezeptor (CAR) ausgestattet – einem kleinen Fühler, der Körperzellen abtastet und nach spezifischen Eigenschaften von Krebszellen sucht. Zurück im Körper des Patienten oder der Patientin, spüren sie das Antigen auf, auf das sie ausgerichtet sind, und töten die Tumorzellen ab.
Die Arbeitsgruppen von Dr. Uta Höpken und Dr. Armin Rehm am Max Delbrück Center haben einen Ansatz für eine neuartige CAR-T-Zelltherapie gegen eine Form des Lymphdrüsenkrebses entwickelt, die von den B‑Lymphozyten ausgeht: B‑Non-Hodgkin-Lymphom. Unter der Leitung von Professor Ulrich Keller und Professor Lars Bullinger von der Charité – Universitätsmedizin Berlin soll die neue Immuntherapie in einer Phase I/IIa-Studie erstmals am Menschen getestet werden. Das gemeinsame Projekt der Charité und des Max Delbrück Center fördert das Bundesministerium für Bildung und Forschung (BMBF) mit 4,6 Millionen Euro. Das Ministerium will Therapien gegen Erkrankungen auf den Weg bringen, die bisher nicht oder nur schwer behandelbar sind.
CXCR5: Für einen CAR kaum zu verfehlen
Die bislang zur Behandlung von Blut- und Lymphknotenkrebs zugelassenen CARs docken zumeist an das Antigen CD19 an, ein Oberflächenmolekül von B‑Zellen, die sich bösartig verändern und zu Krebszellen werden können. Uta Höpken und Armin Rehm haben ein Molekül identifiziert, das sich wahrscheinlich noch besser als Angriffspunkt für einen CAR zur Behandlung von Lymphdrüsenkrebs eignet: CXCR5. Anders als CD19, dessen Menge auf den Krebszellen von Patient*in zu Patient*in unterschiedlich hoch sein oder gar verloren gehen kann, kommt CXCR5 gleichmäßig auf allen reifen Lymphdrüsenkrebszellen vor. Es befindet sich darüber hinaus nicht nur auf den Tumor-B-Zellen, sondern auch auf bestimmten T‑Helferzellen, die das Tumorwachstum unterstützen. „Diese Eigenschaften machen CXCR5 zu einem einzigartigen Ziel für CAR-T-Zelltherapien“, sagt Uta Höpken. In Mausmodellen konnten die Forschenden zeigen, dass die CAR-T-Zellen das CXCR5 besonders zuverlässig finden und die Tumorzellen vernichten.
Ob die neue Immuntherapie sicher und auch bei Menschen wirksam ist, müssen klinische Studien zeigen. Professor Ulrich Keller, Direktor der Medizinischen Klinik mit Schwerpunkt Hämatologie, Onkologie und Tumorimmunologie am Campus Benjamin Franklin, bereitet mit seinem Team erste Untersuchungen mit einigen wenigen ausgewählten Patient*innen vor: „Wir sind zuversichtlich, dass wir mit dieser Phase I‑Studie die Sicherheit der neuen CXCR5-CAR-T-Zelltherapie nachweisen und auch erste Hinweise auf deren Wirksamkeit finden werden. Sowohl die Tumorzelle als auch deren unterstützende Mikroumgebung therapeutisch zu adressieren, ist ein vielversprechender und hochinnovativer Ansatz.“
Sobald das Berliner Landesamt für Gesundheit und Soziales (LAGeSo) die Herstellung des Zellprodukts und das Paul-Ehrlich-Institut (PEI) als Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel die klinische Studie genehmigt haben, beginnt die Rekrutierung von bis zu 24 Patient*innen. Die Wissenschaftler*innen rechnen damit, dass dies Anfang 2024 der Fall sein wird. Eingeschlossen werden zunächst nur Patient*innen, bei denen die Standardtherapie nicht angeschlagen hat.
Text: Jana Ehrhardt-Joswig
- Klinische Studien
-
Neue Arzneimittel werden in einem standardisierten Verfahren auf Sicherheit und Wirksamkeit getestet, bevor sie für die regelhafte Anwendung zugelassen werden. In einer Phase I‑Studie wird ein Therapeutikum – nach umfangreicher Vorprüfung – erstmals beim Menschen angewendet, um vorläufige Daten über die Verträglichkeit und Sicherheit sowie weitere Auswirkungen auf den Organismus zu erhalten. Die Anzahl der Studienteilnehmer*innen ist klein. Treten keine bedenklichen Nebenwirkungen auf und gibt es erste Hinweise auf eine mögliche Wirksamkeit, schließt sich eine Phase II-Studie an. Dabei werden Verträglichkeit und Nebenwirkungen bei einer etwas größeren Anzahl von Patient*innen ermittelt und die Dosierung in Hinblick auf eine mögliche Wirksamkeit optimiert. Erst in Phase III-Studien, die sich oft über Jahre hinziehen und eine große Anzahl von Teilnehmer*innen einschließen, kann der Nachweis der Wirksamkeit der neuen Substanz erbracht werden. Hierzu wird die neue Substanz mit anderen verfügbaren und bereits zugelassenen Medikamenten verglichen. Phase III-Studien liefern die Daten, die für die behördliche Zulassung notwendig sind.
Weiterführende Informationen
Bild zum Download
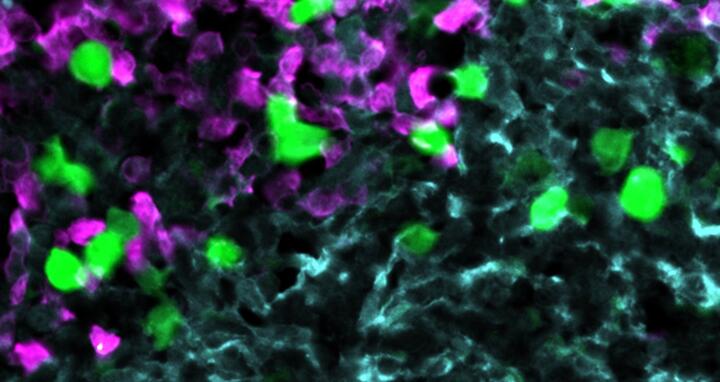
Die gegen CXCR5 gerichteten CAR-T-Zellen (grün) greifen Lymphom-Zellen (rot) innerhalb des Stroma-Zellnetzwerks im B‑Zell-Follikel an (hellblau). Foto: AG Höpken / Rehm, Max Delbrück Center
Kontakte
Dr. Uta Höpken
Leiterin der Arbeitsgruppe „Mikroumgebung als Regulator bei Autoimmunität und Krebs“
Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC)
+49 (0)30 9406 3330
uhoepken@mdc-berlin.de
Dr. Armin Rehm
Leiter der Arbeitsgruppe „Translationale Tumorimmunologie“
Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC)
+49 (0)30 9406 3817
arehm@mdc-berlin.de
Jana Schlütter
Redakteurin, Kommunikation
Max Delbrück Center
+49 (0)30 9406 2121
jana.schluetter@mdc-berlin.de oder presse@mdc-berlin.de
- Max Delbrück Center
-
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (Max Delbrück Center) gehört zu den international führenden biomedizinischen Forschungszentren. Nobelpreisträger Max Delbrück, geboren in Berlin, war ein Begründer der Molekularbiologie. An den Standorten in Berlin-Buch und Mitte analysieren Forscher*innen aus rund 70 Ländern das System Mensch – die Grundlagen des Lebens von seinen kleinsten Bausteinen bis zu organ-übergreifenden Mechanismen. Wenn man versteht, was das dynamische Gleichgewicht in der Zelle, einem Organ oder im ganzen Körper steuert oder stört, kann man Krankheiten vorbeugen, sie früh diagnostizieren und mit passgenauen Therapien stoppen. Die Erkenntnisse der Grundlagenforschung sollen rasch Patient*innen zugutekommen. Das Max Delbrück Center fördert daher Ausgründungen und kooperiert in Netzwerken. Besonders eng sind die Partnerschaften mit der Charité – Universitätsmedizin Berlin im gemeinsamen Experimental and Clinical Research Center (ECRC) und dem Berlin Institute of Health (BIH) in der Charité sowie dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK). Am Max Delbrück Center arbeiten 1800 Menschen. Finanziert wird das 1992 gegründete Max Delbrück Center zu 90 Prozent vom Bund und zu 10 Prozent vom Land Berlin.
- Charité – Universitätsmedizin Berlin
-
Die Charité – Universitätsmedizin Berlin ist mit rund 100 Kliniken und Instituten an vier Campi sowie 3.099 Betten eine der größten Universitätskliniken Europas. Forschung, Lehre und Krankenversorgung sind hier eng miteinander vernetzt. Mit Charité-weit durchschnittlich 20.921 und konzernweit rund 17.615 Beschäftigten aus über 100 Nationen gehört die Berliner Universitätsmedizin zu den größten Arbeitgeberinnen der Hauptstadt. Dabei waren 5.047 der Beschäftigten im Pflegebereich und 4.988 im wissenschaftlichen und ärztlichen Bereich tätig. An der Charité wurden im vergangenen Jahr 123.793 voll- und teilstationäre Fälle sowie 682.731 ambulante Fälle behandelt. Im Jahr 2021 hat die Charité Gesamteinnahmen von rund 2,3 Milliarden Euro, inklusive Drittmitteleinnahmen und Investitionszuschüssen, erzielt. Mit den 215,8 Millionen Euro eingeworbenen Drittmitteln erreichte die Charité einen erneuten Rekord. An der gemeinsamen medizinischen Fakultät von Freier Universität Berlin und Humboldt-Universität zu Berlin, die zu den größten in Deutschland gehört, werden mehr als 9.000 Studierende in Humanmedizin, Zahnmedizin sowie Gesundheitswissenschaften ausgebildet. Darüber hinaus gibt es 730 Ausbildungsplätze in 11 Gesundheitsberufen und 111 Ausbildungsplätze in 8 weiteren Berufen. Die Berliner Universitätsmedizin setzt Akzente in den Forschungsschwerpunkten: Infektion, Inflammation und Immunität einschließlich Forschung zu COVID-19, Kardiovaskuläre Forschung und Metabolismus, Neurowissenschaften, Onkologie, Regenerative Therapien sowie Seltene Erkrankungen und Genetik. Wissenschaftlerinnen und Wissenschaftler der Charité arbeiten unter anderem in 28 DFG-Sonderforschungsbereichen, darunter sieben mit Sprecherfunktion, in drei Exzellenzclustern, davon eines mit Sprecherschaft, 10 Emmy-Noether-Nachwuchsgruppen, 14 Grants des European Research Councils und 8 europäischen Verbundprojekten mit Charité-Koordination.